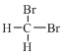题目内容
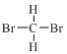
【题目】将![]() 持续通入下列八种饱和溶液:
持续通入下列八种饱和溶液:![]()
![]()
![]()
![]()
![]()
![]() 和NaCl
和NaCl![]() ,最终能得到沉淀、浊液或析出晶体的是
,最终能得到沉淀、浊液或析出晶体的是
A.②⑤⑧B.⑤⑥⑧C.①②③④⑦D.②③④⑧
【答案】C
【解析】
①过量的![]() 通入饱和
通入饱和![]() 溶液中发生反应生成碳酸氢钠,碳酸氢钠溶解性小于碳酸钠,所以有晶体碳酸氢钠析出,故正确;
溶液中发生反应生成碳酸氢钠,碳酸氢钠溶解性小于碳酸钠,所以有晶体碳酸氢钠析出,故正确;
②碳酸的酸性强于硅酸,向硅酸钾溶液中通入二氧化碳生成硅酸沉淀,故正确;
③NaAlO2溶液通入过量的二氧化碳,可生成氢氧化铝沉淀,故正确;
④碳酸的酸性强于苯酚,二氧化碳通入苯酚钠溶液生成苯酚沉淀,故正确;
⑤碳酸的酸性强于次氯酸,过量二氧化碳能够与次氯酸钙反应生成碳酸氢钙,碳酸氢钙易溶于水,故错误;
⑥碳酸的酸性弱于盐酸,与氯化钙不反应,不会产生沉淀,故错误;
⑦可生成碳酸氢钠和氯化铵,为侯氏制碱法原理,发生反应:![]() ,所以有
,所以有![]() 晶体析出,故正确;
晶体析出,故正确;
⑧过量的![]() 与
与![]() 反应生成碳酸氢钙和水,碳酸氢钙溶于水,故错误;
反应生成碳酸氢钙和水,碳酸氢钙溶于水,故错误;
①②③④⑦正确,故选C。

【题目】某学校课外活动小组仅有一大一小两试管和氢氧化钠溶液。甲、乙两个同学找来铝制废牙膏皮,各自设计了一套装置如下图,制取并收集一试管氢气。
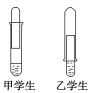
(1)哪个学生设计的装置比较合理?____(填“甲”或“乙”),另一设计装置不合理的原因____________
(2)用比较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是____。
(3)还可以用哪些常见物品和试剂代替废牙膏皮和氢氧化钠溶液完成实验?_____________
(4)测定H2和空气混合气体的爆炸范围实验如下所述。取10支大试管,依次盛水90%(体积分数)、80%……再用排水集气法收集H2,而后分别把试管口移近酒精灯火焰,实验结果如下:
H2体积分数/% | 90 | 80 | 70 | 60~20 | 10 | 5 |
空气体积分数/% | 10 | 20 | 30 | 40~80 | 90 | 95 |
点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱爆炸 | 强爆炸 | 弱爆炸 | 不燃烧 不爆炸 |
由上述实验结果评价:用向下排空气法收集H2,保持试管倒置移近火焰,如果只发出轻微的“噗声”,表示收集的H2已纯净的说法的真正涵义:________________________。