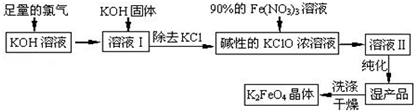
题目内容
7. 利用I2O5可消除CO污染或定量测定CO,反应为:
利用I2O5可消除CO污染或定量测定CO,反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s);△H 1
(1)已知:2CO(g)+O2(g)?2CO2(g);△H 2
2I2(s)+5O2(g)?2I2O5(s);△H 3
则△H 1=2.5△H2-0.5△H3(用含△H 2和△H 3的代数式表示).
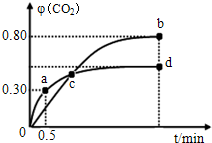
(2)不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2的体积百分数φ(CO2)随时间t变化曲线如图.请回答:
①从反应开始至a点时,CO的平均反应速率为v(CO)=0.6mol•L-1•min-1,
b点时化学平衡常数的表达式Kb=$\frac{{c}^{5}(C{O}_{2})}{{c}^{5}(CO)}$.
②d点时,温度不变,若将容器体积压缩至原来的一半,请在图中补充画出CO2体积分数的变化曲线.
③下列说法正确的是AB.(填字母序号)
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的平均相对分子质量相等
C.增加I2O5的投料量有利于提高CO的转化率
D.b点和d点的化学平衡常数:Kb<Kd.
分析 (1)已知:①2CO(g)+O2(g)?2CO2(g);△H 2
②2I2(s)+5O2(g)?2I2O5(s);△H 3
根据盖斯定律,①×$\frac{5}{2}$-②×$\frac{1}{2}$可得:5CO(g)+I2O5(s)?5CO2(g)+I2(s);
(2)①a点时二氧化碳体积分数为0.3,反应前后气体物质的量不变,则CO2的物质的量为2mol×0.3=0.6mol,由方程式可知转化的CO为0.6mol,再根据v=$\frac{△c}{△t}$计算v(CO);
化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
②d点时,温度不变,若将容器体积压缩至原来的一半,反应前后气体体积不变,平衡不移动,CO2体积分数不变;
③A.所反应进行容器内气体质量增大,容器内气体密度增大,密度不变表明反应达到平衡状态;
B.两种温度下,c点时体系中二氧化碳的体积分数相等,而两种温度下体系中CO2、CO的物质的量之比相等;
C.I2O5为固体,增大其投料量不影响平衡移动;
D.平衡时b点二氧化碳体积分数大,由平衡常数表达式可知b点平衡常数更大.
解答 解:(1)已知:①2CO(g)+O2(g)?2CO2(g)△H 2
②2I2(s)+5O2(g)?2I2O5(s)△H 3
根据盖斯定律,①×$\frac{5}{2}$-②×$\frac{1}{2}$可得:5CO(g)+I2O5(s)?5CO2(g)+I2(s),则△H 1=2.5△H2-0.5△H3,
故答案为:2.5△H2-0.5△H3;
(2)①a点时二氧化碳体积分数为0.3,反应前后气体物质的量不变,则CO2的物质的量为2mol×0.3=0.6mol,由方程式可知转化的CO为0.6mol,故v(CO)=$\frac{\frac{0.6mol}{2L}}{0.5min}$=0.6mol•L-1•min-1;
b点时化学平衡常数的表达式Kb=$\frac{{c}^{5}(C{O}_{2})}{{c}^{5}(CO)}$,
故答案为:0.6mol•L-1•min-1;$\frac{{c}^{5}(C{O}_{2})}{{c}^{5}(CO)}$;
②d点时,温度不变,若将容器体积压缩至原来的一半,反应前后气体体积不变,平衡不移动,CO2体积分数不变,如图所示: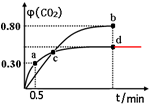 ,
,
故答案为: ;
;
③A.所反应进行容器内气体质量增大,容器内气体密度增大,密度不变表明反应达到平衡状态,故A正确;
B.两种温度下,c点时体系中二氧化碳的体积分数相等,而两种温度下体系中CO2、CO的物质的量之比相等,则平均相对分子质量相等,故B正确;
C.I2O5为固体,增大其投料量不影响平衡移动,CO的转化率不变,故C错误;
D.平衡时b点二氧化碳体积分数大,由平衡常数表达式K=$\frac{{c}^{5}(C{O}_{2})}{{c}^{5}(CO)}$可知b点平衡常数更大,故D错误,
故选:AB.
点评 本题考查化学平衡计算与影响因素、反应速率计算、平衡常数、反应热计算等,需要学生熟练掌握基础知识并灵活应用.

| A. | 氢气与氧气化合生成液态水 | B. | 氯化钠固体溶于水 | ||
| C. | 氧化铁变成Fe2O3 | D. | 水由气态变为液态 |
N2(g)+3H2(g)?2NH3(g)△H<0
(1)若在5min时反应达到平衡,此时测得NH3的物质的量为4mol.则前5min的平均反应速率v(N2)=0.2mol/(L•min).平衡时H2的转化率为50%.该温度下的平衡常数K1=$\frac{4}{27}$(用分数表示);若反应开始时,将1molN2和3molH2通入到该容器,再达新平衡时的平衡常数为K2,则K2=K1(填“>”、“<”或“=”)
(2)平衡后,若要提高H2的转化率,可以采取的措施有C.
A.加了催化剂B.充入一定量的Ne
C.降低反应体系的温度D.再充入2mol的Ne和6mol的H2
(3)其化学平衡常数K与温度T的关系如表所示:
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1>K2(填“>”、“<”或“=”).
②400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数为2,2L的容器中,当测得NH3、N2和H2物质的量分别为6mol、4mol和2mol时,则该反应的v(N2)减>v(N2)增(填“>”、“<”或“=”).
(4)根据化学反应速率和化学平衡理论,联合合成氨的生产实际,你认为下列说法不正确的是C
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益.
 水煤气(CO和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
水煤气(CO和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1(1)该反应的平衡常数的表达式为K=$\frac{c(CO)×c({H}_{2})}{c({H}_{2}O)}$,升高温度K将减小(填“增大”、“减小”或“不变”).
(2)上述反应达到平衡后,将体系中的C (s)全部移走,平衡不移动(填“向左移”、“向右移”或“不移动”).
(3)上述反应在t0时刻达到平衡(如图),若在t1时刻缩小容器体积,请在图中继续画出t1时刻之后正、逆反应速率(ν正、ν逆)随时间的变化:
(4)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
| 容器编号 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | 0.6 | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正>ν逆 |
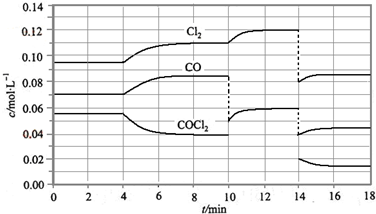
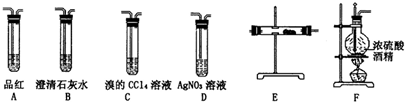 某研究小性学习小组的同学欲用如图所示的装置完成下列实验,验证制得的乙烯气体中含有SO2、CO2、水蒸气;确定乙烯与单质溴能否反应及反应类型.
某研究小性学习小组的同学欲用如图所示的装置完成下列实验,验证制得的乙烯气体中含有SO2、CO2、水蒸气;确定乙烯与单质溴能否反应及反应类型.