题目内容
2. 水煤气(CO和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
水煤气(CO和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1(1)该反应的平衡常数的表达式为K=$\frac{c(CO)×c({H}_{2})}{c({H}_{2}O)}$,升高温度K将减小(填“增大”、“减小”或“不变”).
(2)上述反应达到平衡后,将体系中的C (s)全部移走,平衡不移动(填“向左移”、“向右移”或“不移动”).
(3)上述反应在t0时刻达到平衡(如图),若在t1时刻缩小容器体积,请在图中继续画出t1时刻之后正、逆反应速率(ν正、ν逆)随时间的变化:
(4)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
| 容器编号 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | 0.6 | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正>ν逆 |
分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
正反应为吸热反应,升高温度平衡逆向移动,平衡常数减小;
(2)上述反应达到平衡后,将体系中的C(s)全部移走,不影响水、CO、氢气浓度变化,平衡不移动;
(3)若在t1时刻缩小容器体积,压强增大,瞬间正、逆反应速率都增大,平衡逆向移动,逆反应速率增大更多;
(4)Ⅰ、Ⅱ处于平衡状态,根据I计算平衡常数K,结合平衡常数计算Ⅱ中c(H2);
计算Ⅲ中此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行,进而判断ν正、ν逆相对大小.
解答 解:(1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出,C (s)+H2O(g)?CO (g)+H2 (g)的平衡常数表达式K=$\frac{c(CO)×c({H}_{2})}{c({H}_{2}O)}$;
正反应为吸热反应,升高温度平衡逆向移动,平衡常数减小,
故答案为:$\frac{c(CO)×c({H}_{2})}{c({H}_{2}O)}$;减小;
(2)上述反应达到平衡后,将体系中的C(s)全部移走,不影响水、CO、氢气浓度变化,平衡不移动,故答案为:不移动;
(3)若在t1时刻缩小容器体积,压强增大,瞬间正、逆反应速率都增大,平衡逆向移动,逆反应速率增大更多,t1时刻之后正、逆反应速率(ν正、ν逆)随时间的变化: ,故答案为:
,故答案为: ;
;
(4)Ⅰ、Ⅱ处于平衡状态,根据I可知平衡常数K=$\frac{0.6×0.1}{0.6}$=0.1,则Ⅱ中$\frac{0.2×c({H}_{2})}{0.12}$=0.1,故c(H2)=0.6mol/L;
Ⅲ中浓度商Qc=$\frac{0.2×0.4}{0.1}$=0.8>K=1,反应向逆反应进行,则ν正>ν逆,
故答案为:0.6;>.
点评 本题考查化学平衡影响因素、平衡常数及应用等,注意理解掌握平衡常数应用,难度中等.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. | 1.5mol FeCl2 | B. | 1.5mol FeCl3 | ||
| C. | 1.5mol Fe | D. | 1L 1.5mol•L-1 Fe2(SO4)3溶液 |
| A. | 该反应的化学平衡常数表达式是K=$\frac{{{(C)}^{4}(D)}^{2}}{{{(A)}^{3}(B)}^{2}}$ | |
| B. | 此时,B的平衡转化率是40% | |
| C. | 增大该体系的压强,平衡向右移动,化学平衡常数增大 | |
| D. | 增加B,平衡向右移动,B的平衡转化率增大 |
| A. | 参加反应的水的质量是加入的Al的质量的2倍 | |
| B. | 反应中放出的气体在标准状况下的体积为2.24L | |
| C. | 所得溶液中Na+和Al3+的物质的量之比为2:1 | |
| D. | 所得溶液中阳离子和阴离子的物质的量之比为2:1 |
 在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,G的水溶液是一种常用的漂白剂.(反应中生成的水和部分反应条件未列出)
在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,G的水溶液是一种常用的漂白剂.(反应中生成的水和部分反应条件未列出) .
.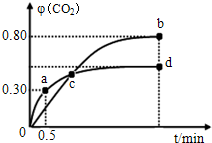 利用I2O5可消除CO污染或定量测定CO,反应为:
利用I2O5可消除CO污染或定量测定CO,反应为: