题目内容
20.将2.0mol SO2气体和2.0mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )| A. | 1.6 mol SO2+0.3 mol O2+0.4 mol SO3 | |
| B. | 3.0 mol SO2+0.5 mol O2+1.0 mol SO3 | |
| C. | 3.0 mol SO2+1.0 mol O2+1.0 mol SO3 | |
| D. | 4.0 mol SO2+1.0 mol O2+0.1 mol SO3 |
分析 开始投入2.0mol SO2气体和2.0mol SO3气体,等效为开始投入4.0mol SO2气体和1mol O2气体,在恒温恒容下,平衡时SO3的物质的量不变为n mol,说明应是完全等效平衡,按化学计量转化到左边,对应成分的物质的量相同,即满足4.0mol SO2气体和1mol O2气体,据此判断.
解答 解:加入2.0mol SO2气体和2.0mol SO3气体,等效为开始投入4.0mol SO2气体和1mol O2气体,在恒温恒容下,平衡时SO3的物质的量不变为n mol,说明应是完全等效平衡,按化学计量转化到左边,对应成分的物质的量相同,即满足4.0mol SO2气体和1mol O2气体,
A、开始为1.6 mol SO2+0.3 mol O2+0.4 mol SO3,转化到左边,由2SO2(g)+O2(g)?2SO3(g)可知,n(SO2)=1.6mol+0.4 mol=2mol,n(O2)=0.3mol+0.5×0.4mol=0.5mol,不满足4.0mol SO2气体和1mol O2气体,故A错误;
B、开始为3.0 mol SO2+0.5 mol O2+1.0 mol SO3,转化到左边,由2SO2(g)+O2(g)?2SO3(g)可知,n(SO2)=3.0mol+1.0mol=4mol,n(O2)=0.5mol+0.5×1.0mol=1mol,满足4.0mol SO2气体和1mol O2气体与原平衡等效,故B正确;
C、开始为3.0 mol SO2+1.0 mol O2+1.0 mol SO3,转化到左边,由2SO2(g)+O2(g)?2SO3(g)可知,n(SO2)=3.0mol+1.0mol=4mol,n(O2)=1.0mol+0.5×1.0mol=1.5mol,不满足4.0molSO2气体和1molO2气体,故C错误;
D、开始为4.0 mol SO2+1.0 mol O2+0.1 mol SO3,转化到左边,由2SO2(g)+O2(g)?2SO3(g)可知,n(SO2)=4mol+0.1mol=4.1mol,n(O2)=1mol+0.5×0.1mol=1.05mol,不满足4.0molSO2气体和1molO2气体,故D错误;
故选B.
点评 本题考查化学平衡计算、等效平衡等,难度中等,清楚等效平衡规律是解题的关键.

| A. | 甲烷分子是正方形分子 | |
| B. | 乙烯是平面形结构 | |
| C. | 乙炔分子中的4个原子在同一条直线上 | |
| D. | 丙炔的三个碳原子在同一直线上 |
| A. | 苯、乙酸、四氯化碳 | B. | 乙醇、乙醛、乙酸 | ||
| C. | 乙醛、乙二醇、甲酸 | D. | 乙酸乙酯、乙醇、甘油 |
| A. | 18.75g | B. | 18.59g | C. | 26.1g | D. | 26.33g |
| A. | Na在氧气中燃烧主要生成Na2O | |
| B. | 将CO2通入次氯酸钙溶液可生成次氯酸 | |
| C. | 将SO2通入BaCl2溶液可生成BaSO3沉淀 | |
| D. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
| A. | 乙醇 | B. | 葡萄糖 | C. | 甘油 | D. | 氨基酸 |
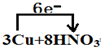 ═3Cu(NO3)2+2NO↑+4H2O,还原剂是Cu,氧化剂是硝酸;(填化学式)
═3Cu(NO3)2+2NO↑+4H2O,还原剂是Cu,氧化剂是硝酸;(填化学式)