题目内容
3.700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2+H2(g)
| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 反应在t1min内的平均速率为v(H2)=0.40/t1mol•L-1•min-1 | |
| B. | 保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)=0.40 mol | |
| C. | 保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小 | |
| D. | 温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
分析 A.根据v=$\frac{△c}{△t}$计算v(CO),结合化学反应速率之比等于化学计量数之比计算v(H2);
B.CO与H2O按物质的量比1:1反应,充入0.60 mol CO和1.20 mol H2O与充入1.20 mol CO和0.6mol H2O到达平衡时对应生成物的浓度、物质的量相同;
C.保持其他条件不变,增加一种反应物的浓度,平衡向正反应方向移动,另一种反应物的转化率增大;
D.根据平衡时各物质的浓度计算700℃时的平衡常数,比较不同温度下的平衡常数大小可判断反应的吸放热.
解答 解:A.v(CO)=$\frac{\frac{1.2-0.8}{2}}{t{\;}_{1}}$=$\frac{0.2}{t{\;}_{1}}$mol/(L•min),化学反应速率之比等于化学计量数之比,则v(H2)=v(CO)=$\frac{0.2}{t{\;}_{1}}$mol/(L•min),故A错误;
B.CO与H2O按物质的量比1:1反应,充入0.60 mol CO和1.20 mol H2O与充入1.20 mol CO和0.6mol H2O,平衡时生成物的浓度对应相同,t1min时n(CO)=0.8mol,n(H2O)=0.6mol-0.4mol=0.2mol,t2min时n(H2O)=0.2mol,说明t1min时反应已经达到平衡状态,根据化学方程式可知,则生成的n(CO2)=0.4mol,故B正确;
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,平衡向右移动,达到新平衡时CO转化率增大,H2O转化率减小,H2O的体积分数会增大,故C错误;
D.t1min时反应已经达到平衡状态,此时c(CO)=$\frac{0.8mol}{2L}$=0.4mol/L,c(H2O)=$\frac{0.2mol}{2L}$=0.1mol/L,c(CO2)=c(H2)=$\frac{0.4mol}{2L}$=0.2mol/L,则k=$\frac{0.2×0.2}{0.4×0.1}$=1,温度升至800℃,上述反应平衡常数为0.64,说明温度升高,平衡是向左移动的,那么正反应应为放热反应,故D错误;
故选B.
点评 本题属于化学平衡问题,主要考查学生对速率概念与计算,平衡常数概念与计算,平衡移动等有关内容理解和掌握程度,题目难度中等,注意C选项中的规律利用.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 2:3 | B. | 1:3 | C. | 1:1 | D. | 1:2 |
| A. | 10℃20 mL 3 mol•L-1的盐酸溶液 | B. | 20℃30 mL 2 mol•L-1的盐酸溶液 | ||
| C. | 20℃20 mL 2 mol•L-1的盐酸溶液 | D. | 20℃10 mL 4 mol•L-1的盐酸溶液 |
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| C. | 向NaAlO2溶液中通入过量CO2:2 AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
| A. | 硅与任何酸都不反应 | |
| B. | 硅是构成矿物岩石的主要原料,其化合态硅几乎全部是硅石(成份为SiO2)和硅酸盐 | |
| C. | 硅的性质很稳定,能以游离态存在于自然界 | |
| D. | 常温时硅不与任何物质反应 |
| A. | CH3OH(g)+O2(g)═H2O(1)+CO2(g)+2H+(aq)+2e - | |
| B. | O2(g)+4H+(aq)+4e -═2H2C(1) | |
| C. | CH3OH(g)+H2O(1)═CO2(g)+6H+(aq)+6e - | |
| D. | O2(g)+2H2O(1)+4e -═4OH - |
| A. | 甲苯和环己烯都能使酸性高锰酸钾溶液褪色 | |
| B. | 用银氨溶液可以鉴别乙醛和麦芽糖溶液 | |
| C. | 甲醛和乙二醇都可作为合成高分子化合物的单体 | |
| D. | 丙烷和2-甲基丙烷的一氯代物均为两种 |
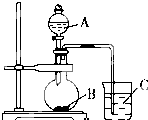 某化学小组设计实验元素周期表中元素的性质,请回答下列问题
某化学小组设计实验元素周期表中元素的性质,请回答下列问题