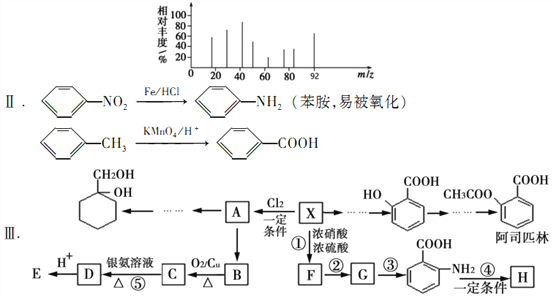
��Ŀ����
����Ŀ���¶�ΪT1ʱ���������ݻ���Ϊ1L�ĺ����ܱ������н�������Ӧ: 2NO2(g)![]() 2NO(g)+O2(g) (����Ӧ����)��ʵ����:v��=v(NO2)����=k��c2(NO2)��v��=v(NO)����= 2v(O2)����=k��c2(NO)��c(O2)��k����k��Ϊ���ʳ��������¶�Ӱ�졣
2NO(g)+O2(g) (����Ӧ����)��ʵ����:v��=v(NO2)����=k��c2(NO2)��v��=v(NO)����= 2v(O2)����=k��c2(NO)��c(O2)��k����k��Ϊ���ʳ��������¶�Ӱ�졣
����˵����ȷ����
���� ��� | ���ʵ���ʼŨ�ȣ�mol��L��1�� | ���ʵ�ƽ��Ũ�ȣ�mol��L��1�� | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
�� | 0.6 | 0 | 0 | 0.2 |
�� | 0.3 | 0.5 | 0.2 | |
�� | 0 | 0.5 | 0.35 | |
A. ��kΪ�÷�Ӧ�Ļ�ѧƽ�ⳣ��������k=k��:k��
B. ��ƽ��ʱ�����������������е���ѹǿ֮��Ϊ20��17
C. ����������ʼƽ�������ƶ�����ƽ��ʱ����������NO2��ת���ʱ��������е�С
D. ���ı��¶�ΪT2,��T2>T1,��k��:k��<0.8
���𰸡�C
��������ƽ��ʱ�������淴Ӧ������ȣ�����![]() ������K=c2(NO)c(O2)/c2(NO2)= k��/ k����A���������ݷ�Ӧ����ʽ����������
������K=c2(NO)c(O2)/c2(NO2)= k��/ k����A���������ݷ�Ӧ����ʽ����������![]() ��ƽ��Ũ�ȿ�֪��ƽ��ʱ��c(NO)=0.4 mol��L��1��c(NO2)=0.2 mol��L��1����
��ƽ��Ũ�ȿ�֪��ƽ��ʱ��c(NO)=0.4 mol��L��1��c(NO2)=0.2 mol��L��1����![]() �¶��£��÷�Ӧ��ƽ�ⳣ��
�¶��£��÷�Ӧ��ƽ�ⳣ��![]() ����������Ũ����QC=0.2��0.52/0.32=0.56<0.8,��Ӧ�����ƶ����������������1mol,���������з�Ӧ������������������С��0.85mol�����Դ�ƽ��ʱ�����������������е���ѹǿ֮�ȴ���20��17��B����������������ڷ�Ӧ��֪��NO2��ת����Ϊ0.4/0.6=2/3,������������NO2��ת����ҲΪ2/3����Ӧ������У���÷�Ӧ��ƽ�ⳣ��Ϊ��
����������Ũ����QC=0.2��0.52/0.32=0.56<0.8,��Ӧ�����ƶ����������������1mol,���������з�Ӧ������������������С��0.85mol�����Դ�ƽ��ʱ�����������������е���ѹǿ֮�ȴ���20��17��B����������������ڷ�Ӧ��֪��NO2��ת����Ϊ0.4/0.6=2/3,������������NO2��ת����ҲΪ2/3����Ӧ������У���÷�Ӧ��ƽ�ⳣ��Ϊ��
2NO2(g)![]() 2NO(g)+O2(g)
2NO(g)+O2(g)
��ʼ�� 0.3 0.5 0.2
�仯�� 0.2 0.2 0.1
ƽ���� 0.1 0.7 0.3
ƽ�ⳣ��Ϊk=0.3��0.72/0.12=14.7>8,������������NO2��ת����С��2/3��������������ʼƽ�������ƶ�����ƽ��ʱ����������NO2��ת���ʱ��������е�С��C��ȷ�����ڸ÷�Ӧ����Ӧ�����ȷ�Ӧ���¶�![]() ������
������![]() ʱƽ�ⳣ��������k��:k��>0.8����ȷѡ��C��
ʱƽ�ⳣ��������k��:k��>0.8����ȷѡ��C��

 ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�����Ŀ����ҵ���Է�ˮ�е�Cr2O72-��ת��ΪCr3+��ȥ��ʵ�����õ�ⷨģ��ù��̣�������±���ʾ(ʵ�鿪ʼʱ��Һ���Ϊ50mL,Cr2O72-����ʼŨ�ȡ���ѹ�����ʱ�����ͬ)������˵���У�����ȷ����
ʵ�� | �� | �� | �� |
������� | ����������Ϊʯī | ����������Ϊʯī�� �μ�1mLŨ���� | ����Ϊʯī������Ϊ�����μ�1mLŨ���� |
Cr2O72-��ȥ����/% | 0.922 | 12.7 | 57.3 |
A. �Ա�ʵ��٢ڿ�֪������pH�������Cr2O72-��ȥ����
B. ʵ����У�Cr2O72-�������ŵ�ĵ缫��Ӧʽ��Cr2O72-+6e-+14H+�T2Cr3++7H2O
C. ʵ����У�Cr2O72-ȥ������ߵ�ԭ����Cr2O72-+6 Fe2++14H+�T2Cr3++6Fe3++7H2O
D. ʵ����У������ϵ�·��ÿͨ��6mol���ӣ�����1molCr2O72-����ԭ