题目内容
已知Cl有两种天然同位素35Cl、37Cl,Cl的相对原子质量为35.5,Na只有一种原子23Na,求10吨纯度为90%的食盐(杂质中不含Na、Cl)样品中含37Cl多少吨,含Na35Cl多少吨.
考点:同位素及其应用
专题:原子组成与结构专题
分析:元素的相对原子质量为该元素各种核素的相对原子质量的平均值,原子的相对原子质量在数值上等于其质量数,先根据元素的相对原子质量计算3517Cl和3717Cl的原子个数比,再根据原子个数比和质量守恒计算23Na35Cl、23Na37Cl的质量.
解答:
解:氯元素的相对原子质量35.5是质量数分别为35和37的核素的平均值,可以采用十字交叉法计算其原子个数比;
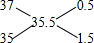 ,3717Cl和3517Cl的原子个数之比为0.5:1.5=1:3,10吨纯度为90%的食盐中食盐的质量为10吨×90%=9吨,设23Na35Cl、23Na37Cl的质量分别为X、Y吨,则X+Y=9(质量守恒),
,3717Cl和3517Cl的原子个数之比为0.5:1.5=1:3,10吨纯度为90%的食盐中食盐的质量为10吨×90%=9吨,设23Na35Cl、23Na37Cl的质量分别为X、Y吨,则X+Y=9(质量守恒),
:
=
(Cl的原子个数之比),解得:X≈6.692吨,Y≈2.308吨,所以含3717Cl的质量=2.308吨×
≈1.423吨;
答:样品中含37Cl1.423吨;含Na35Cl6.692吨;
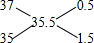 ,3717Cl和3517Cl的原子个数之比为0.5:1.5=1:3,10吨纯度为90%的食盐中食盐的质量为10吨×90%=9吨,设23Na35Cl、23Na37Cl的质量分别为X、Y吨,则X+Y=9(质量守恒),
,3717Cl和3517Cl的原子个数之比为0.5:1.5=1:3,10吨纯度为90%的食盐中食盐的质量为10吨×90%=9吨,设23Na35Cl、23Na37Cl的质量分别为X、Y吨,则X+Y=9(质量守恒),| X |
| 58 |
| Y |
| 60 |
| 3 |
| 1 |
| 37 |
| 60 |
答:样品中含37Cl1.423吨;含Na35Cl6.692吨;
点评:本题以计算核素的质量为载体考查了同位素原子个数的计算,题目难度中等,明确元素的相对原子质量为该元素各种核素的相对原子质量的平均值是解本题的关键.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
有关铝及其化合物的说法错误的是( )
| A、铁易生锈,而铝在空气中较稳定,所以铁比铝活泼 |
| B、铝能在空气中稳定存在是因为其表面覆盖着一层保护膜 |
| C、氧化铝是一种难溶物质,是一种较好的耐火材料 |
| D、氢氧化铝能中和胃酸,可用于制胃药 |
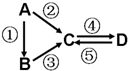
观察下列几个装置示意图,有关叙述错误的是( )


| A、装置①中烧杯内中加入黄色的K3[Fe(CN)6]溶液,一段时间后看不到Fe电极附近有蓝色沉淀生成,该装置可看作金属的析氢腐蚀 |
| B、装置②盐桥中的Cl-向硫酸铜溶液移动 |
| C、装置③中外电路电流方向:b极→a极 |
| D、装置④中阳极反应:2Cl--2e-═Cl2↑ |
下列关于有机物的叙述,错误的是( )
| A、乙烯能使溴水和酸性KMnO4溶液褪色 |
| B、体积分数为75%的酒精溶液会使细菌蛋白质变性 |
| C、1mol甲烷和1mol氯气在光照条件下充分反应,生成1mol CH3Cl |
| D、CH3CH2CH2CH3和CH3CH(CH3)2互为同分异构体 |
 Ⅰ;现有如下物质:①酒精、②铜、③氢氧化钡、④氨气、⑤蔗糖、⑥高氯酸、⑦碳酸氢钠、⑧磷酸、⑨硫化氢、⑩Al2(SO4)3.请用物质的序号填写下列空白:
Ⅰ;现有如下物质:①酒精、②铜、③氢氧化钡、④氨气、⑤蔗糖、⑥高氯酸、⑦碳酸氢钠、⑧磷酸、⑨硫化氢、⑩Al2(SO4)3.请用物质的序号填写下列空白: (1)与N元素同周期的第一电离能最大且电负性最小的元素的基态原子核外电子排布式为
(1)与N元素同周期的第一电离能最大且电负性最小的元素的基态原子核外电子排布式为