题目内容
6.下列关于纯净物、混合物、强电解质、弱电解质和非电解质的组合正确的是( )| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 氨水 | 氯水 | 硫酸 | 醋酸 | 干 冰 |
| B | 氧化铁 | 盐酸 | 硫酸钡 | 亚 硫酸 | 二氧化硫 |
| C | 胆矾 | 碘酒 | 苛性钾 | 氢硫酸 | 碳酸钙 |
| D | 氯化氢 | 氢氧化钠溶液 | 氯化钠 | 磷酸 | 氯气 |
| A. | A | B. | B | C. | C | D. | D |
分析 纯净物:有一种物质组成,包括单质和化合物;混合物:由两种或两种以上的物质组成;在水溶液里或熔融状态下完全电离的是强电解质,部分电离的是弱电解质;在水溶液里或熔融状态下不导电的化合物是非电解质,电解质和非电解质都是化合物来分析.
解答 解:A.氨水、氯水、硫酸、醋酸、干冰,分别属于混合物、混合物、强电解质、弱电解质、非电解质,故A错误;
B.氧化铁、盐酸、硫酸钡、亚硫酸、二氧化硫分别属于纯净物、混合物、强电解质、弱电解质、非电解质,故B正确;
C.胆矾、碘酒、苛性钾、氢硫酸、碳酸钙分别是纯净物、混合物、强电解质、弱电解质、强电解质,故C错误;
D.氯化氢、氢氧化钠溶液、氯化钠、磷酸、氯气,分别是纯净物、混合物、强电解质、弱电解质、单质,故D错误;
故选:B.
点评 本题考查了纯净物、混合物、电解质、非电解质的概念判断,熟悉相关概念是解题关键,注意电解质、非电解质都是化合物,题目难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
16.下列有关实验操作正确的是( )
| A. |  除去Cl2中的HCl 除去Cl2中的HCl | B. | 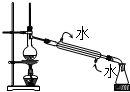 制备蒸馏水 制备蒸馏水 | ||
| C. |  萃取碘水中碘 萃取碘水中碘 | D. |  称量氢氧化钠固体 称量氢氧化钠固体 |
17.一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(保持温度不变),下列说法正确的是( )


| A. | 右边CO与CO2分子数之比为3:1 | |
| B. | 右侧CO的质量为2.75g | |
| C. | 右侧气体密度是相同条件下氧气密度的16倍 | |
| D. | 若改变右边CO和CO2的充入量而使隔板处于距离右端1/6处,保持温度不变,则前后两次充入情况容器内的压强之比为24:25 |
14.下列叙述中正确的是( )
| A. | 将SO2通入酸性高锰酸钾溶液中,溶液褪色,不能说明SO2具有漂白性 | |
| B. | 浓盐酸和浓硫酸暴露在空气中浓度都会降低,其原因相同 | |
| C. | 向某无色溶液中滴加氯化钡溶液,产生白色沉淀,再加入稀盐酸后该沉淀不溶解,说明原溶液中一定含有SO42- | |
| D. | 土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性 |
1.下列说法中正确的是( )
| A. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃的条件下△H不相同 | |
| B. | 化学反应中的能量变化都表现为热量变化 | |
| C. | 任何放热反应在常温下都能发生 | |
| D. | 化学反应的反应热可通过反应物的键能之和减去生成物的键能之和求得 |
18.如图的装置为实验室模拟铜的精练.以下叙述正确的是( )
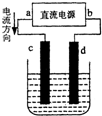

| A. | c为纯铜,d为粗铜 | |
| B. | 实验前,铜片可用热碱溶液除油渍,盐酸除铜绿 | |
| C. | 用含Cu2+的盐配成电解质溶液,电解后其浓度保持不变 | |
| D. | 若阴极得到2摩尔电子,则阳极质量减少64克 |
 根据如图回答问题:
根据如图回答问题: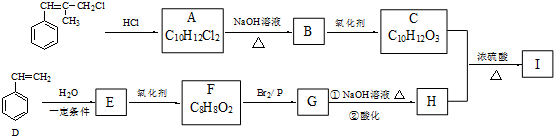
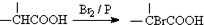
 .
. .
.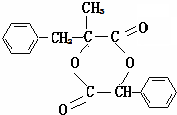 .
. (写结构简式).
(写结构简式).