题目内容
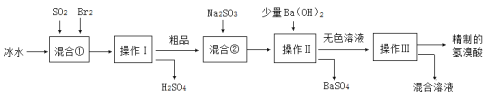
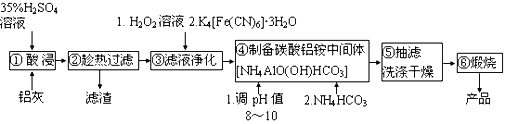
【题目】铝生产加工过程中产生大量的铝灰,直接掩埋造成铝资源浪费,还会带来严重的污染。某铝厂的铝灰经分析所含主要物质如下:Al、Al2O3、AlN、SiO2、Fe2O3,其他杂质均不溶于稀硫酸。如图是酸浸法用该铝灰生产高纯氧化铝的生产流程:
已知:i.Fe3+ +K++ [Fe(CN)6]4-=K[Fe(CN)6Fe]↓
ii.AlN常温下与水缓慢反应,酸性或碱性条件下反应较快
iii.NH4AlO(OH)HCO3难溶于碱性溶液和乙醇
请回答:
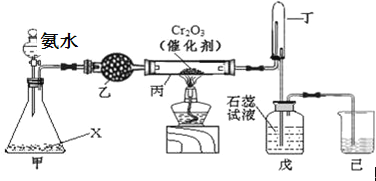
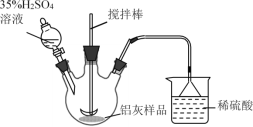
(1)实验室模拟工业生产①酸浸步骤的装置如图,该装置的不合理之处为____。
(2)步骤③加入H2O2溶液的目的是________________。
(3)步骤④调节pH最合适的试剂是________________。
A.NaOH B.H2SO4 C.NH3·H2O D.Ca(OH)2
(4)步骤⑤吸滤瓶内液体高度快达到支管口位置时应拔掉瓶上橡皮管,_______,洗涤沉淀操作为_______________。
(5)写出煅烧碳酸铝铵中间体得到高纯氧化铝的化学方程式______________。
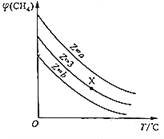
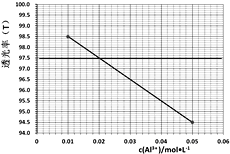
(6)已知Al3+对光的吸收与其浓度成线性关系,色度计传感器可以测量某种波长的光穿过溶液的透射率确定溶液浓度。如图是红色光照下透光率(T)对应c(Al3+)的标准曲线。为测定铝灰中铝元素的回收率,准确称取0.5000g铝灰(折合铝元素含量60.00%)进行制备高纯氧化铝的实验,将所制得的粉末与固体NaOH反应后加水溶解、过滤,滤液定容到250mL容量瓶中。用移液管移取25.00mL到锥形瓶中,加2滴指示剂,滴加稀盐酸至溶液体积变为50.00mL,NaAlO2恰好反应生成AlCl3。取该溶液于比色皿中进行色度检测,测得溶液透光率为97.5,则铝元素的回收率=_________。
【答案】尾气无法用稀硫酸完全吸收或可燃性气体未处理 将Fe2+氧化为Fe3+,便于形成沉淀除去 C 从吸滤瓶上口倒出滤液 往过滤器中加水至没过沉淀,待水滤出后,重复操作2~3次,直至滤液检验不出SO42-,再用少量乙醇淋洗 2NH4AlO(OH)HCO3![]() Al2O3+2NH3↑+3H2O+2CO2↑ 90.0%
Al2O3+2NH3↑+3H2O+2CO2↑ 90.0%
【解析】
(1)根据反应原理,观察反应装置和尾气处理装置,找出不合理之处;
(2)流程中步骤③是为了把铁离子转变为沉淀除去,那么加入H2O2溶液的目的也是与之关联的,分析铁元素的存在形态就可确定双氧水的作用;
(3)步骤④调节pH最合适的试剂是谁?从反应的角度、不引入杂质离子的角度分析选择;
(4)步骤⑤的操作要抓住其要点简答;
(5)煅烧碳酸铝铵中间体得到的产物,除了高纯氧化铝外,其余产物可以结合酸式碳酸盐分解规律、不溶性碱分解规律、铵盐非氧化还原分解规律获得并据此写化学方程式;
(6)获得相关数据及题目提供的信息,可计算铝元素的回收率;
(1) 铝灰经分析所含主要物质如下:Al、Al2O3、AlN、SiO2、Fe2O3,在搅拌下,铝灰和从分液漏斗加入的硫酸反应,产生的气体有氨气、氢气等,可见装置中尾气无法用稀硫酸完全吸收或可燃性气体氢气未处理;
答案为:尾气无法用稀硫酸完全吸收或可燃性气体未处理;
(2)流程中步骤③是为了把杂质中铁元素转变为沉淀除去,有大量铝情况下,溶液中有铁离子存在、也有亚铁离子,则加入绿色氧化剂H2O2溶液的目的是将Fe2+氧化为Fe3+,便于形成沉淀除去;
答案为:将Fe2+氧化为Fe3+,便于形成沉淀除去;
(3)步骤④要制备NH4AlO(OH)HCO3,信息iii显示——NH4AlO(OH)HCO3难溶于碱性溶液,故要把酸性溶液调节成弱碱性,则可用碱性物质调节pH,为了避免引入新杂质最合适的试剂是氨水,则选C;
答案为:C;
(4)步骤⑤是用抽滤法分离出碳酸铝铵中间体,吸滤瓶内液体高度快达到支管口位置时应拔掉瓶上橡皮管,从吸滤瓶上口倒出滤液;而洗涤沉淀的操作则为:往过滤器中加水至没过沉淀,待水滤出后,重复操作2~3次,直至滤液检验不出SO42-,再用少量乙醇淋洗,便于快速得到纯净干燥的固体(因为信息iii,NH4AlO(OH)HCO3难溶于碱性溶液和乙醇);
答案为:从吸滤瓶上口倒出滤液;往过滤器中加水至没过沉淀,待水滤出后,重复操作2~3次,直至滤液检验不出SO42-,再用少量乙醇淋洗;
(5)煅烧碳酸铝铵中间体得到的产物,除了高纯氧化铝外,其余产物分别为氨气、二氧化碳和水,则化学方程式为2NH4AlO(OH)HCO3![]() Al2O3+2NH3↑+3H2O+2CO2↑;
Al2O3+2NH3↑+3H2O+2CO2↑;
答案为:2NH4AlO(OH)HCO3![]() Al2O3+2NH3↑+3H2O+2CO2↑;
Al2O3+2NH3↑+3H2O+2CO2↑;
(6)由图知,透光率为97.5时,溶液中铝离子的浓度为0.02mol/L,则结合其它相关数据,铝元素的回收率= ;
;
答案为:90.0%。

 灵星计算小达人系列答案
灵星计算小达人系列答案