题目内容
已知A、B为单质,C为化合物。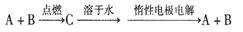
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C溶液中滴加过量NaOH溶液,先出现浑浊后澄清,则B可能为Al
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
能实现上述转化关系的是
A.①② B.②④ C.①③ D.③④
B
解析试题分析:从 转化关系可知,电解电解质溶液时,是电解电解质本身,因此C可以为不活泼金属的无氧酸盐或无氧酸.
转化关系可知,电解电解质溶液时,是电解电解质本身,因此C可以为不活泼金属的无氧酸盐或无氧酸.
①若A为钠,则B为氧气,则C为过氧化钠,C的水溶液为氢氧化钠,电解氢氧化钠得到氢气和氧气,不符合转化关系,故①错误;
②若C的溶液遇Na2CO3,放出CO2气体,则C可以为HCl、HBr、HI等,电解这些酸的水溶液实际上是电解本身,在阴极得到氢气,故A可能是H2,
B可能为卤素单质,故②符号上述转化关系,故②正确;
③若C的溶液中滴加KSCN溶液显红色,则C中含铁离子,电解铁盐不会得到铁单质,故③错误;
④由C的溶液中滴加NaOH溶液有蓝色沉淀生成,则C为铜盐,C可以为卤化铜,如氯化铜、溴化铜等,电解他们的水溶液都会得到铜和卤素单质,故B可以为铜,故④正确.
故选B。
考点:考查无机推断。

 阅读快车系列答案
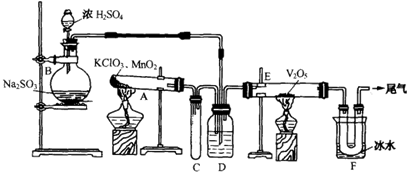
阅读快车系列答案某化学小组进行Na2SO3的性质实验探究。
(1)在白色点滴板的a、b、c三个凹槽中滴有Na2SO3溶液,再分别滴加下图所示的试剂: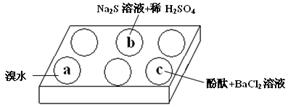
实验现象如下表:
| 编号 | 实验现象 |
| a | 溴水褪色 |
| b | 产生淡黄色沉淀 |
| c | 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去 |
根据实验现象进行分析:
① a中实验现象证明Na2SO3具有 性。
② b中发生反应的离子方程式是 。
③ 应用化学平衡原理解释c中现象(用化学用语及简单文字表述) 。
(2)在用NaOH 溶液吸收SO2的过程中,往往得到Na2SO3和NaHSO3的混合溶液,溶液pH 随n(SO32-):n(HSO3-) 变化关系如下表:
| n(SO32—): n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
① 当吸收液中n(SO32-):n(HSO3-) ="10:1" 时,溶液中离子浓度关系正确的是 (填字母)。
A.c(Na+) +c(H+) = 2c(SO32-) +c(HSO3-) + c(OH-)
B.c(Na+) > c(HSO3-) > c(SO32-) > c(OH-)>c(H+)
C.c(Na+) > c(SO32-) > c(HSO3-) > c(OH-)>c(H+)
②若n(SO32-):n(HSO3-) = 3:2,则0.8 mol NaOH溶液吸收了标准状况下的SO2 L。
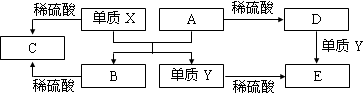
已知某物质X能发生如下转化:
下列有关上述转化关系中物质及其反应的叙述错误的是
| A.若X为N2或NH3(催化氧化),则A为硝酸 |
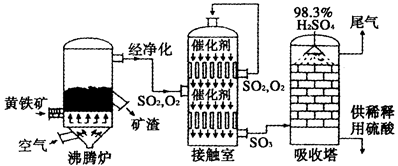
| B.若X为S 或H2S(完全燃烧),则A为硫酸 |
| C.若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y |
| D.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: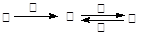 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
| A.若甲为焦炭,则丁可能是O2 |
| B.若甲为SO2,则丁可能是氨水 |
| C.若甲为Fe,则丁可能是盐酸 |
| D.若甲为NaOH溶液,则丁可能是CO2 |
现有H2SO4、Ba(OH)2、Na2CO3和氯水四种溶液,有如图所示的相互关系,图中每条线段两端的物质可以发生化学反应。下列推断合理的是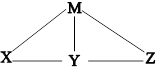
| A.M一定是Ba(OH)2 | B.Y可能是氯水 |
| C.X一定是Na2CO3溶液 | D.Z可能是H2SO4 |
 Fe2O3 + 2Al
Fe2O3 + 2Al