题目内容
15.能说明醋酸是弱电解质的事实是( )| A. | 醋酸溶液的导电性比盐酸弱 | |
| B. | 0.1mol/LCH3COOH溶液中,氢离子浓度约为0.001mol/L | |
| C. | 醋酸溶液用水稀释后,氢离子浓度下降 | |
| D. | 醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 |
分析 证明醋酸是弱电解质的方法有:根据其强碱盐的酸碱性、根据相同物质的量浓度的盐酸溶液导电性强弱、根据一定物质的量浓度的醋酸溶液的pH大小判断等.
解答 解:A.醋酸和盐酸的物质的量浓度相对大小未知,所以不能根据溶液导电性强弱判断醋酸电离程度,则不能证明醋酸是弱电解质,故A错误;
B.0.1mol/LCH3COOH溶液中,氢离子浓度约为0.001mol/L,说明醋酸分子部分电离,属于弱电解质,故B正确;
C.无论醋酸是强电解质还是弱电解质,醋酸溶液稀释后氢离子浓度都下降,所以不能据此判断醋酸电离程度,则不能说明醋酸是弱电解质,故C错误;
D.醋酸和碳酸钙反应生成二氧化碳,只能说明醋酸酸性大于碳酸,不能证明醋酸部分电离,所以不能证明醋酸是弱电解质,故D错误;
故选:B.
点评 本题考查电解质强弱的判断,明确强电解质与弱电解质的本质区别:是否完全电离是解题关键,题目难度不大.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
5.如图是课外活动小组设计的用化学电源使LED灯发光的装置.下列说法错误的是( )
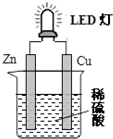

| A. | 如果将硫酸换成柠檬汁,导线中不会有电子流动 | |
| B. | 装置中存在“化学能→电能→光能”的转换 | |
| C. | 铜片表面有气泡生成 | |
| D. | 如果将锌片换成铁片,电路中的电流方向不变 |
6.下列各物质中,互为同系物的是( )
| A. | CH3-CH2-CH2-CH3与 | B. | 醋酸和硬脂酸(C17H35COOH) | ||
| C. | 硝基苯和三硝基甲苯 | D. | CH3CH2Cl 和CH2ClCH2CH2Cl |
7.下列各组有机物,只用水就可以鉴别出来的是( )
| A. | 己烷、己烯、己炔 | B. | 苯、己烯、乙醇 | C. | 溴苯、乙醇和甲苯 | D. | 硝基苯、苯和甲苯 |
9.下列物质中,不能使溴的四氯化碳溶液和高锰酸钾酸性溶液褪色的是( )
| A. | C5H12 | B. | 丙烯 | C. | C2H4 | D. | 乙炔 |
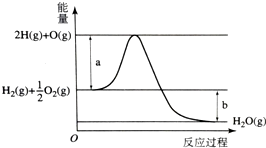 已知H2O(g)=H2(g)+$\frac{1}{2}$O2(g),反应过程中能量变化如图所示.请回答下列问题:
已知H2O(g)=H2(g)+$\frac{1}{2}$O2(g),反应过程中能量变化如图所示.请回答下列问题: 在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化的情况如图:
在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化的情况如图: