题目内容
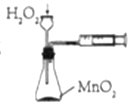
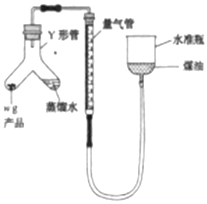
【题目】用下图装置可以测定混合气体中ClO2的含量:
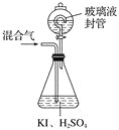
Ⅰ.在锥形瓶中加入足量的碘化钾,用50mL水溶解后,再加入3mL稀硫酸;
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中;
Ⅴ.用0.100 0mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
(1)锥形瓶内ClO2与碘化钾反应的离子方程式为____________________________。
(2)玻璃液封装置的作用是_______________________。
(3)V中加入的指示剂通常为_____,滴定至终点的现象是_______。
(4)测得混合气中ClO2的质量为________ g。
【答案】2ClO2+10I-+8H+=2Cl-+5I2+4H2O 吸收残留的ClO2气体(避免碘的逸出) 淀粉溶液 溶液由蓝色变为无色,且半分钟内溶液颜色不再改变 0.027 00
【解析】
(1)由题目信息可知,ClO2通入锥形瓶与酸性碘化钾溶液反应,氧化I-为I2,自身被还原为Cl-,同时生成水;
(2)玻璃液封装置可防止有害气体逸出;
(3)淀粉遇碘单质变蓝;
(4)由关系式2ClO2![]() 5I2
5I2![]() 10S2O32-可求。
10S2O32-可求。
(1)由分析可知,ClO2氧化I-为I2,自身被还原为Cl-,同时生成水,反应离子方程式为2ClO2+10I-+8H+═2Cl-+5I2+4H2O;
(2) ClO2气体易溶于水,玻璃液封装置的作用是吸收残留的ClO2气体(避免碘的逸出);
(3)V中加入的指示剂通常为淀粉溶液,滴定至终点的现象是溶液由蓝色变为无色,且半分钟内不变色;
(4)由关系式2ClO2![]() 5I2
5I2![]() 10S2O32-,则m(ClO2)=
10S2O32-,则m(ClO2)=![]() =0.027 00g。
=0.027 00g。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案