题目内容
【题目】某化学兴趣小组在实验室探究过渡金属元素化合物的性质
I、铁及其化合物
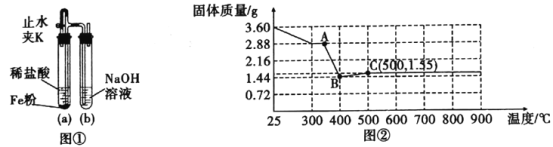
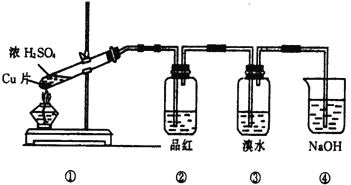
(1)向FeSO4溶液中滴加NaOH溶液,产生白色沉淀,但迅速变为灰绿色,最终变为红褐色,为顺利看到较长时间的白色沉淀,设计了图①装置:①检查装置气密性,装入药品;②打开止水夹K;③在试管b出口收集气体并验纯;④关闭止水夹K。以上操作正确的顺序是:___。
(2)某实验小组称量3.60 g草酸亚铁晶体(FeC2O4·2H2O)加热过程中,固体质量变化如图②所示:
①请写出AB段发生反应的化学方程式:___。②C点成分为:___。
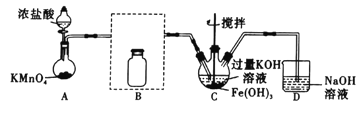
(3)向FeCl3溶液中加入过量Na2SO3溶液,设计实验证明两者发生了氧化还原反应并且为可逆反应。(简要说明实验步骤、现象和结论,仪器和药品自选)___。
II、铜及其化合物
向2ml0.2mol·L-1Na2SO3溶液中滴加0.2mol·L-1CuSO4溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。
已知:Cu+![]() Cu+Cu2+,Cu2+
Cu+Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
(4)用稀硫酸证实沉淀中含有Cu+的实验现象是___。
(5)向洗净的棕黄色沉淀中加入足量KI溶液,产生白色沉淀,继续向上层清液中加入淀粉溶液并没有变蓝的现象出现,请结合离子反应方程式解释不变蓝的原因___。
【答案】①②③④ FeC2O4![]() FeO+CO↑+CO2↑ Fe3O4 取反应后的溶液分成两份,一份滴加KSCN溶液,变血红色;另一份加K3[Fe(CN)6]溶液,产生特征蓝色沉淀即可说明; 有暗红色不溶物生成 I2+SO32-+H2O=2I-+SO42-+2H+
FeO+CO↑+CO2↑ Fe3O4 取反应后的溶液分成两份,一份滴加KSCN溶液,变血红色;另一份加K3[Fe(CN)6]溶液,产生特征蓝色沉淀即可说明; 有暗红色不溶物生成 I2+SO32-+H2O=2I-+SO42-+2H+
【解析】
(1) ①检查装置气密性,装入药品;②打开止水夹K;③在试管b出口收集气体并验纯;④关闭止水夹K;
(2)由图像计算可知A点结晶水已完全失去,继续加热草酸亚铁开始分解产生铁的氧化物,根据铁元素质量守恒可计算B点固体成分为FeO;FeO不稳定,在空气中加热变为Fe3O4;
(3)利用Fe2+的生成说明发生氧化还原反应,利用Fe3+不足却有剩余说明为可逆反应;
(4)注意沉淀本身有Cu2+的干扰;
(5)碘被Na2SO3还原为I-。
(1) 为顺利看到较长时间的白色沉淀,操作正确的顺序是:①检查装置气密性,装入药品;②打开止水夹K;③在试管b出口收集气体并验纯;④关闭止水夹K;
答案为①②③④;
(2)由图像计算可知A点结晶水已完全失去,继续加热草酸亚铁开始分解产生铁的氧化物,根据铁元素质量守恒可计算B点固体成分为FeO;①AB段发生反应的化学方程式为:FeC2O4![]() FeO+CO↑+CO2↑;
FeO+CO↑+CO2↑;
②FeO不稳定,在空气中加热变为Fe3O4,故C点成分为Fe3O4;
(3)利用Fe2+的生成说明发生氧化还原反应,利用Fe3+不足却有剩余说明为可逆反应;答案为取反应后的溶液分成两份,一份滴加KSCN溶液,变血红色;另一份加K3[Fe(CN)6]溶液,产生特征蓝色沉淀即可说明;
(4)注意沉淀本身有Cu2+的干扰;用稀硫酸证实沉淀中含有Cu+的实验现象是有暗红色不溶物生成;
(5)碘被Na2SO3还原为I-,发生反应的离子方程式为I2+SO32-+H2O=2I-+SO42-+2H+。