题目内容
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是

A. 该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数
B. 500℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-2a kJ·mol-l
2SO3(g) ΔH=-2a kJ·mol-l
C. 该反应中,反应物的总键能小于生成物的总键能
D. ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热
【答案】B
【解析】试题分析:由图可知,该反应正反应为放热反应。A. 该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数,A正确;B. 500℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应放热akJ,由于该反应为可逆反应,得不到1mol SO3(g),所以热化学方程式2SO2(g)+O2(g)![]() 2SO3(g) 的反应热不等于-2akJ·mol-l,B不正确;C. 该反应中为放热反应,其ΔH<0,所以反应物的总键能小于生成物的总键能,C正确;D. ΔH=E1-E2,使用催化剂能改变反应的活化能,但不改变反应热,D正确。本题选B。
2SO3(g) 的反应热不等于-2akJ·mol-l,B不正确;C. 该反应中为放热反应,其ΔH<0,所以反应物的总键能小于生成物的总键能,C正确;D. ΔH=E1-E2,使用催化剂能改变反应的活化能,但不改变反应热,D正确。本题选B。

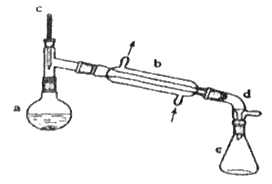
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全。确定分解产物的成分。
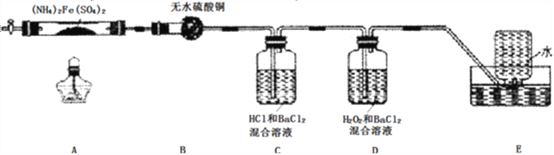
(1)B装置的作用是________________________________。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中定有______气体产生,写出D中发生反应的离子方程式____________________。若去掉C,是否能得出同样结论并解释其原因__________________________。
(3)A中固体分解后产生NH3,写出其两种用途________________________________________。
(4)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3而不含FeO。请完成表内容。(试剂,仪器自选)
实验步骤 | 预期现象 | 结论 |
①取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解; ②______________________________________________________ | 固体残留物仅为Fe2O3 |
(5) 用实验的方法验证C溶液含有NH4+___________________________________________。