题目内容
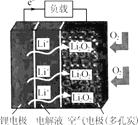
【题目】已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在。现以Al—H2O2电池电解尿素CO(NH2)2的碱性溶液制备H2,下列说法不正确的是( )
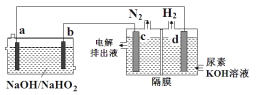
A.电解过程中,电子的流向由a→d→c→b
B.电池的正极反应为:HO2-+2e-+H2O=3OH-
C.电解时,消耗5.4gAl,则产生标况下2.24L N2
D.电极c是阳极,且反应后该电极区pH减小
【答案】A
【解析】
根据装置,左侧为电池,右侧为电解池,d电极上产生H2,根据电解原理,d电极为阴极,则c电极为阳极,a为负极,b为正极,据此分析;
A、根据装置,左侧为电池,右侧为电解池,d电极上产生H2,根据电解原理,d电极为阴极,则c电极为阳极,a为负极,b为正极,电解质内部没有电子通过,电子流向由a→d,c→b,故A说法错误;
B、根据A选项分析,b电极为正极,电极反应方程式为HO2-+2e-+H2O=3OH-,故B说法正确;
C、根据得失电子数目守恒,因此有![]() ,解得V(N2)=2.24L,故C说法正确;
,解得V(N2)=2.24L,故C说法正确;
D、根据A选项分析,电极c为阳极,电极反应式为CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O,消耗OH-,反应后该电极区pH减小,故D说法正确;
答案为A。

练习册系列答案
相关题目