题目内容
【题目】对SCN-的性质进行探究,设计了以下实验
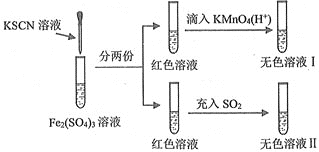
已知:(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质均与卤素单质相似。下列说法正确的是( )
A.溶液颜色变红时发生反应的离子方程式是:Fe3++3SCN-=Fe(SCN)3↓
B.红色溶液褪色表现了SO2的漂白性
C.氧化性:KMnO4>Fe3+>(SCN)2
D.无色溶液Ⅱ中滴入适量的KMnO4(H+)溶液,溶液又变成红色
【答案】D
【解析】
A.![]() 不是沉淀,溶液颜色变红时发生反应的离子方程式是:
不是沉淀,溶液颜色变红时发生反应的离子方程式是:![]() ,故A错误;
,故A错误;
B.充入二氧化硫,红色溶液变无色溶液,说明三价铁离子被还原为二价铁离子,表现了二氧化硫的还原性,故B错误;
C.![]() 溶液可将
溶液可将![]() 氧化为
氧化为![]() ,而
,而![]() 不能将
不能将![]() 氧化为
氧化为![]() ,则
,则![]() ,故C错误;
,故C错误;
D.无色溶液Ⅱ中含有二价铁离子,滴入适量的![]() 溶液,又产生三价铁离子,则溶液又变成红色,故D正确。
溶液,又产生三价铁离子,则溶液又变成红色,故D正确。
故选:D。

练习册系列答案
相关题目
【题目】下表为元素周期表的一部分。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
一 | ① | ||||||
二 | ② | ③ | ④ | ⑤ | ⑥ | ||
三 | ⑦ | ⑧ | ⑨ | ⑩ | |||
四 | |||||||
(1)表中元素__
(2)表中元素⑦的原子结构示意图为__,在周期表中的位置为____
(3)表中元素⑥⑩的氢化物的稳定性顺序为__(填写化学式,下同)。
(4)表中元素⑩的最高价氧化物对应水化物的酸性:__。
(5)表中元素②和⑦的最高价氧化物对应水化物的碱性:__。