题目内容
已知25℃时几种物质的电离程度(溶液浓度为0.1mol?L-1)如下表:(已知H2SO4第一步电离是完全的)
(1)25℃时,0.1mol?L-1上述几种溶液中c(H+)由大到小的顺序是(填序号,下同) .
(2)25℃时,pH相同的上述几种溶液,其物质的量浓度由大到小的顺序是 .
(3)25℃时,将足量的锌粉投入等体积,pH等于1的上述几种溶液中,产生H2的体积(同温同压下)由大到小的顺序是 .
(4)25℃时,0.1mol?L-1?H2SO4溶液中HSO4-的电离程度小于0.1mol?L-1?NaHSO4溶液中HSO4-的电离程度的原因是 .
| ①H2SO4溶液中的HSO4- | ②NaHSO4溶液中的HSO4- | ③CH3COOH | ④HCl |
| 10% | 29% | 1.33% | 100% |
(2)25℃时,pH相同的上述几种溶液,其物质的量浓度由大到小的顺序是
(3)25℃时,将足量的锌粉投入等体积,pH等于1的上述几种溶液中,产生H2的体积(同温同压下)由大到小的顺序是
(4)25℃时,0.1mol?L-1?H2SO4溶液中HSO4-的电离程度小于0.1mol?L-1?NaHSO4溶液中HSO4-的电离程度的原因是
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)c(H+)=c(酸)×α(电离度),注意硫酸分两步电离;
(2)等pH的酸,其电离程度越大,酸的物质的量浓度越小;
(3)等pH的酸,其电离程度越大,酸的物质的量浓度越小,根据氢原子守恒,由氢元素的物质的量计算生成氢气的体积大小;
(4)电离时含有相同的离子能抑制酸电离.
(2)等pH的酸,其电离程度越大,酸的物质的量浓度越小;
(3)等pH的酸,其电离程度越大,酸的物质的量浓度越小,根据氢原子守恒,由氢元素的物质的量计算生成氢气的体积大小;
(4)电离时含有相同的离子能抑制酸电离.
解答:
解:(1)硫酸第一步完全电离,第二步部分电离,硫酸中c(H+)=(0.1+0.1×10%)mol/L=0.11mol/L;
硫酸氢钠溶液中,cH+)=(0.1×29%)mol/L=0.029mol/L;
醋酸溶液中,c(H+)=(0.1×1.33%)mol/L=0.00133mol/L;
盐酸溶液中,c(H+)=0.1mol/L;
所以c(H+)由大到小的顺序是①④②③,故答案为:①④②③;
(2)等pH的酸,其电离程度越大,酸的物质的量浓度越小,则物质的量浓度由大到小的顺序是③>②>④>①;
故答案为:③>②>④>①;
(3)等体积pH=1的上述几种溶液中,氢元素的物质的量由大到小的顺序是③②①④,则生成氢气的体积③②①④,
故答案为:③②①④;
(4)硫酸溶液中,硫酸第一步电离出氢离子,第二步又电离出氢离子,第一步电离出的氢离子抑制了第二步的电离,而硫酸氢钠溶液中硫酸氢根离子只有一步电离,所以.1mol/L H2SO4中的HSO4-的电离度小于0.1mol/L NaHSO4中HSO4-的电离度,
故答案为:硫酸的第一步电离抑制了硫酸氢根离子的电离.
硫酸氢钠溶液中,cH+)=(0.1×29%)mol/L=0.029mol/L;
醋酸溶液中,c(H+)=(0.1×1.33%)mol/L=0.00133mol/L;
盐酸溶液中,c(H+)=0.1mol/L;
所以c(H+)由大到小的顺序是①④②③,故答案为:①④②③;
(2)等pH的酸,其电离程度越大,酸的物质的量浓度越小,则物质的量浓度由大到小的顺序是③>②>④>①;
故答案为:③>②>④>①;
(3)等体积pH=1的上述几种溶液中,氢元素的物质的量由大到小的顺序是③②①④,则生成氢气的体积③②①④,
故答案为:③②①④;
(4)硫酸溶液中,硫酸第一步电离出氢离子,第二步又电离出氢离子,第一步电离出的氢离子抑制了第二步的电离,而硫酸氢钠溶液中硫酸氢根离子只有一步电离,所以.1mol/L H2SO4中的HSO4-的电离度小于0.1mol/L NaHSO4中HSO4-的电离度,
故答案为:硫酸的第一步电离抑制了硫酸氢根离子的电离.
点评:本题考查了二元酸的电离方程式、离子浓度的求算、盐的水解规律的应用、离子浓度的比较、电离平衡常数的计算等,题目涉及的知识点较多,侧重反应原理的应用的考查,题目难度中等.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、纤维素、淀粉和蛋白质都是高分子化合物 |
| B、食盐、醋酸和蔗糖都是电解质 |
| C、甲烷和乙烯均可使酸性KMnO4溶液褪色 |
| D、乙酸乙酯和植物油均可水解生成乙醇 |
下列有关化学研究的正确说法是( )
| A、同时改变两个变量来研究反应速率的变化,能更快得出有关规律 |
| B、对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
| C、Na2O2、H2O2所含化学键完全相同,都能作供氧剂 |
| D、根据氧化物的组成元素将氧化物分成酸性氧化物碱性氧化物和两性氧化物 |
下列物质的体积一定是22.4L的是( )
| A、1mol水蒸气 |
| B、17g氨气 |
| C、标准状况下44g二氧化碳 |
| D、0℃2×105Pa压强时2g氢气 |
意大利科学家最近合成了一种新型的氧分子,其化学式为O4,对其说法正确的是( )
| A、O4是一种化合物 |
| B、O4是由O2组成的混合物 |
| C、O4是一种单质 |
| D、一个O4分子由2个O2分子构成 |
反应3H2(g)+N2(g)?2NH3(g)△H=-46.19kJ?mol-1,关于这个反应的平衡常数K,下列说法正确的是( )
| A、随温度升高K增加 |
| B、随压强升高K增加 |
| C、随温度升高K减小 |
| D、随压强升高K减小 |
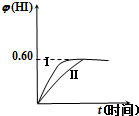 将1mol I2(g)和2mol H2(g)置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)△H<0,并达到平衡.HI的体积分数φ(HI) 随时间的变化如曲线(Ⅱ)所示.
将1mol I2(g)和2mol H2(g)置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)△H<0,并达到平衡.HI的体积分数φ(HI) 随时间的变化如曲线(Ⅱ)所示.