题目内容
【题目】运用化学反应原理研究化学反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) ![]() 2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
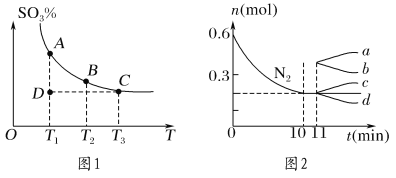
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡________(填“向左”“向右”或“不”)移动。
②若反应进行到状态D时,v逆 ________ (填“>”“<”或“=”)v正。
(2)课本里介绍的合成氨技术叫哈伯法:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,应用此法反应达到平衡时反应物的转化率不高。
2NH3(g) ΔH<0,应用此法反应达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是________(填编号)。
A.使用更高效的催化剂 B.增大压强
C.及时分离出氨气 D.升高温度
②若在某温度下,2 L的密闭容器中发生合成氨的反应,图2表示N2的物质的量随时间的变化曲线。用NH3表示0~10 min内该反应的平均速率v(NH3)=______________;从第11 min起,升高温度,则n(N2)的变化曲线为________(填编号)。
【答案】向左 < B 0.04mol·L-1 ·min-1 c
【解析】
(1)①若在恒温、恒压条件下向上述平衡体系中通入氦气,容器体积变大,浓度减小,相当于减小压强,平衡向体积增大即平衡向左移动。
②从D到A点,即增大三氧化硫的量,则正向移动。
(2)①使用更高效的催化剂,速率增大,但平衡不移动;增大压强速率增大,平衡正向移动;及时分离出氨气,速率减慢;升高温度速率增大,平衡向吸热即逆向移动。
②先求而出氮气速率,再求氨气速率,再根据平衡移动,得到氮气的物质的量变化曲线。
(1)①若在恒温、恒压条件下向上述平衡体系中通入氦气,容器体积变大,浓度减小,相当于减小压强,平衡向体积增大即平衡向左移动,故答案为:向左。
②若反应进行到状态D时,向A点移动,即增大三氧化硫的量,则正向移动,因此v逆 < v正,故答案为:<。
(2)①A选项,使用更高效的催化剂,速率增大,但平衡不移动,故A不符合题意;
B选项,增大压强速率增大,平衡正向移动,故B符合题意;
C选项,及时分离出氨气,速率减慢,故C不符合题意;
D选项,升高温度速率增大,平衡向吸热即逆向移动,故D不符合题意。
综上所述,答案为B。
②若在某温度下,2 L的密闭容器中发生合成氨的反应,图2表示N2的物质的量随时间的变化曲线。![]() ,则反应的平均速率v(NH3)=2 v(N2) = 2×0.02mol·L-1 ·min-1 =0.04mol·L-1 ·min-1;从第11 min起,升高温度,平衡逆向移动,氮气量增加,因此n(N2)的变化曲线为c,故答案为:0.04mol·L-1 ·min-1;c。
,则反应的平均速率v(NH3)=2 v(N2) = 2×0.02mol·L-1 ·min-1 =0.04mol·L-1 ·min-1;从第11 min起,升高温度,平衡逆向移动,氮气量增加,因此n(N2)的变化曲线为c,故答案为:0.04mol·L-1 ·min-1;c。

【题目】.甲胺铅碘(CH3NH3PbI3)可用作全固态钙钛矿敏化太阳能电池的敏化剂,该物质可由甲胺(CH3NH2)、PbI2 及 HI 为原料来合成。请回答下列问题:
(1)制取甲胺的反应为 CH3OH(g)+NH3(g)==CH3NH2(g)+H2O(g),已知该反应中相关化学键的键能数据如下表所示:
共价键 | C-O | H-O | N-H | C-N |
键能/(kJ | 351 | 463 | 393 | 293 |
则该反应的△H=_____kJ·mol-1
(2)工业上利用水煤气合成甲醇的反应为 CO(g)+2H2(g) ![]() CH3OH(g) △H<0。一定温度下, 向体积为 2L 的密闭容器中加入 CO 和 H2,5min 末反应达到化学平衡状态,测得各组分浓度如下表所示。
CH3OH(g) △H<0。一定温度下, 向体积为 2L 的密闭容器中加入 CO 和 H2,5min 末反应达到化学平衡状态,测得各组分浓度如下表所示。
物质 | CO | H2 | CH3OH |
浓度/(mol | 0.9 | 1.0 | 0.6 |
①0~5min 内,用 CO 表示的平均反应速率为_____。
②既能加快反应速率,又能提高氢气转化率的措施有_____(答一条即可)。
③能说明上述反应已达化学平衡状态的是_____(填字母)。
A.v正 (CO)=2v逆 (H2)
B.混合气体密度保持不变
C.反应容器内压强保持不变
D.混合气体的平均摩尔质量不变
(3)PbI2 可由 Pb3O4 和 HI 反应制备,反应的化学方程式为_____。
(4)常温下 PbI2 饱和溶液中 c(I-)=2.0×10-3mol·L-1,则 Ksp(PbI2)=________;已知Ksp(PbS)=4.0×10-28,则反应 PbI2(s)+2-(aq) ![]() PbS(s)+2I-(aq)的平衡常数K=_______________________。
PbS(s)+2I-(aq)的平衡常数K=_______________________。
(5)HI 的分解反应曲线和液相法制备 HI 的反应曲线分别如图 1 和图 2 所示:
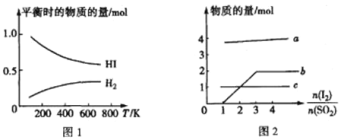
①反应 H2(g)+I2(g)![]() 2HI(g)的△H__________(填“>”或“<")0。
2HI(g)的△H__________(填“>”或“<")0。
②将 SO2 通入碘水中会发生反应:SO2+I2+2H2O==4H++SO42-+2I-,I2+I- ![]() I3-。图 2 中曲线 b 所代表的微粒是_____(填微粒符号)。
I3-。图 2 中曲线 b 所代表的微粒是_____(填微粒符号)。