题目内容
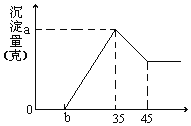
【题目】准确称取6g铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mL 稀H2SO4溶液的烧杯中,充分反应后过滤去掉沉淀,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量和加入的NaOH溶液的体积(mL)如图所示。试回答下列问题:
(1)硫酸溶液的物质的量浓度。___
(2)若b=2.3时,求Al2O3和Fe2O3的质量分数。___、___
【答案】1.75mol/L 85% 12%
【解析】
(1)当加入NaOH溶液的体积为35ml时,n(NaOH)=0.035L×10mol/L=0.35mol,
此时沉淀的质量达到最大值,则此时溶液的溶质只有Na2SO4,根据Na元素守恒有n(Na2SO4)=![]() n(NaOH)=
n(NaOH)=![]() ×0.35mol=0.175mol,根据硫酸根守恒,则有:n(H2SO4)=0.175mol,所以原硫酸溶液中c(H2SO4)=
×0.35mol=0.175mol,根据硫酸根守恒,则有:n(H2SO4)=0.175mol,所以原硫酸溶液中c(H2SO4)=![]() =1.75mol/L,故答案为:稀硫酸溶液的物质的量浓度为1.75mol/L;
=1.75mol/L,故答案为:稀硫酸溶液的物质的量浓度为1.75mol/L;
(2)从35mL~45mL加入的10mL氢氧化钠完全溶解氢氧化铝,该阶段消耗的n(NaOH)=0.01L×10mol/L=0.1mol,根据方程式Al(OH)3+NaOH=NaAlO2+2H2O可知,n[Al(OH)3]=0.1mol,故溶液中n(Al3+)=0.1mol,n(Al2O3)=0.05mol,其质量为0.05mol×102g/mol=5.1g,故Al2O3的质量分数为![]() ×100%=85%;铝离子完全沉淀消耗的氢氧化钠为0.1mol×3=0.3mol,铁离子、铝离子完全消耗的氢氧化钠溶液的体积为35mL﹣2.3mL=32.7mL,故该阶段消耗n(NaOH)=0.0327L×10mol/L=0.327mol,故铁离子完全沉淀消耗的氢氧化钠为0.327mol﹣0.3mol=0.027mol,故n(Fe3+)=
×100%=85%;铝离子完全沉淀消耗的氢氧化钠为0.1mol×3=0.3mol,铁离子、铝离子完全消耗的氢氧化钠溶液的体积为35mL﹣2.3mL=32.7mL,故该阶段消耗n(NaOH)=0.0327L×10mol/L=0.327mol,故铁离子完全沉淀消耗的氢氧化钠为0.327mol﹣0.3mol=0.027mol,故n(Fe3+)=![]() =0.009mol,故m(Fe2O3)=0.009mol×
=0.009mol,故m(Fe2O3)=0.009mol×![]() ×160g/mol=0.72g,故Fe2O3的质量分数为
×160g/mol=0.72g,故Fe2O3的质量分数为![]() ×100%=12%,
×100%=12%,
故答案为: 85%;12%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为MnO2)制备硫酸锰及电解其溶液制锰的工艺流程图:
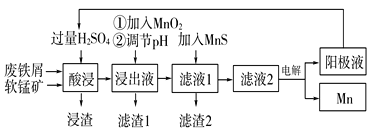
已知:①浸出液中主要含有Fe3+、Fe2+、Co2+、Ni2+等杂质金属离子;
②生成氢氧化物的pH见下表:
物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
开始沉淀的pH | 7.5 | 2.7 | 7.7 | 7.6 | 8.3 |
完全沉淀的pH | 9.7 | 3.7 | 8.4 | 8.2 | 9.8 |
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是____。
(2)流程图中“①加入MnO2”的作用____,MnO2还可以用其他试剂____(填化学式)代替。
(3)流程图中“②调节pH”可以除去某种金属离子,应将溶液pH调节控制的范围是___~7.6。上述流程中,能循环使用的一种物质是___(填化学式)。
(4)向滤液Ⅰ中加入MnS的作用是除去Co2+、Ni2+等离子,其中可以发生反应为MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)等。当该反应完全后,滤液2中的Mn2+与Ni2+的物质的量浓度之比是___[已知Ksp(MnS)=2.8×10-10,Ksp(NiS)=2.0×10-21]。
(5)在适当条件下,在MnSO4、H2SO4和H2O为体系的电解液中电解也可获得MnO2,其阳极电极反应式为____。
(6)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___。
时,z=___。
【题目】某学生对Na2SO3与AgNO3在不同pH下的反应进行探究。
(1)测得Na2SO3溶液pH=10,AgNO3溶液pH=5,原因是(用离子方程式表示):___。
(2)调节pH,实验记录如下:
实验序号 | pH | 实验现象 |
a | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
b | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
c | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质X |
查阅资料得知:
ⅰ.Ag2SO3:白色,难溶于水,溶于过量的Na2SO3溶液。
ⅱ.Ag2O:棕黑色,不溶于水,能和酸反应。
该学生对产生的白色沉淀提出了两种假设:
①白色沉淀为Ag2SO3。
②白色沉淀为Ag2SO4,推测的依据是___。
(3)取b、c中白色沉淀,置于Na2SO3溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是Ag2SO4。实验方法是:另取Ag2SO4固体置于__溶液中,未溶解。
(4)将c中X滤出、洗净,为确认其组成,实验如下:
Ⅰ.向X中滴加稀盐酸,无明显变化。
Ⅱ.向X中加入过量浓HNO3,产生红棕色气体。
Ⅲ.分别用Ba(NO3)2、BaCl2溶液检验Ⅱ中反应后的溶液,前者无明显变化,后者产生白色沉淀。
①实验Ⅰ的目的是___。
②根据实验现象分析,X的成分是___。
③Ⅱ中反应的化学方程式是___。
(5)该同学综合以上实验,分析产生X的原因:随着酸性的增强,体系的还原性增强。