题目内容
20.1.204×1023个NH4+的物质的量为0.2mol,质量为3.6g.分析 根据n(NH4+)=$\frac{N}{{N}_{A}}$计算铵根离子物质的量,根据m=nM计算铵根离子质量.
解答 解:n(NH4+)=$\frac{N}{{N}_{A}}$=$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}/mol}$=0.2mol,m(NH4+)=nM=0.2mol×18g/mol=3.6g,
故答案为:0.2;3.6.
点评 本题考查物质的量有关计算,为高频考点,侧重考查学生计算能力,明确物质的量公式中各个物理量之间的关系式即可解答,题目难度不大.

练习册系列答案
相关题目
10.近年以来,我国多地频现种种极端天气,二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素.
(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
①请结合上表数据,写出NO与活性炭反应的化学方程式C+2NO?N2+CO2.
②上述反应的平衡常数表达式K=$\frac{c(N{\;}_{2})c(CO{\;}_{2})}{c(NO){\;}^{2}}$,根据上述信息判断,T1和T2的关系是C.
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd.
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示
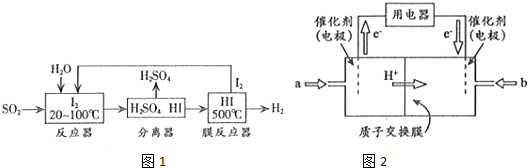
①用离子方程式表示反应器中发生的反应:SO2+I2+2H2O=SO42-+2I-+4H+.
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行.
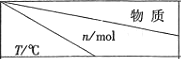
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
 | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应的平衡常数表达式K=$\frac{c(N{\;}_{2})c(CO{\;}_{2})}{c(NO){\;}^{2}}$,根据上述信息判断,T1和T2的关系是C.
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd.
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示

①用离子方程式表示反应器中发生的反应:SO2+I2+2H2O=SO42-+2I-+4H+.
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行.
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
11.有关物质性质或用途的说法正确的是( )
| A. | 浓硫酸具有强氧化性,故不可用作干燥二氧化硫气体 | |
| B. | 明矾可用作净水剂、晶体硅用来制作光导纤维 | |
| C. | 稀硫酸中加入KNO3可使金属铜溶解 | |
| D. | 氯气通入品红溶液中溶液褪色,说明Cl2具有漂白性 |
4.化学与工农业生产和人类生活密切相关,下列说法中正确的是( )
| A. | 超高分辨荧光显微技术能观察到纳米尺度,故能看见化学键的断裂与形成 | |
| B. | 把粉末状的氢化钛泡沫剂添加到熔融的金属铝中,冷却后可得到强度大、质量轻的金属泡沫,利用该金属泡沫可以建造海上漂浮城市 | |
| C. | 煤液化的途径之一是将煤转化为CO和N2再合成甲醚 | |
| D. | 向汽油中添加乙醇后,该混合燃料的热值不变,但可以达到减排的目的 |
 ;w属于非极性 (填“极性”或“非极性)分子;
;w属于非极性 (填“极性”或“非极性)分子;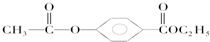 .A经①②两步反应得到C、D和E.B经①②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示.
.A经①②两步反应得到C、D和E.B经①②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示.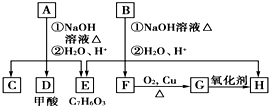
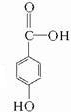 .
.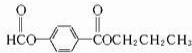 和
和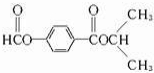 .
.