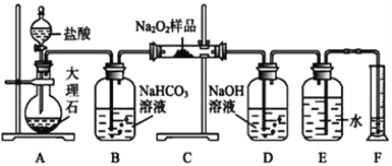
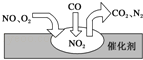
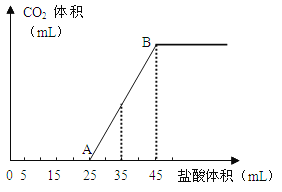
��Ŀ����
����Ŀ����֪:��Cl2ͨ������KOH��Һ��,�����п��ܺ���KCl��KClO��KClO3,��![]() ��ֵ���¶ȸߵ��йء���n(KOH)=a molʱ,����˵������ȷ����
��ֵ���¶ȸߵ��йء���n(KOH)=a molʱ,����˵������ȷ����
A.�μӷ�Ӧ�����������ʵ�������![]() a mol
a mol
B.�ı��¶�,������KClO3��������۲���Ϊ![]() a mol
a mol
C.�ı��¶�,��Ӧ��ת�Ƶ��ӵ����ʵ���n(e-)�ķ�ΧΪ![]() a mol��n(e-)��
a mol��n(e-)��![]() a mol
a mol
D.��ij�¶���,��Ӧ��![]() =11,����Һ��
=11,����Һ��![]() =
=![]()
���𰸡�B
��������
Cl2��KOH�����绯��Ӧ�������·���Cl2��2KOH=KCl��KClO��H2O���¶ȸ�ʱ����3Cl2��6KOH=5KCl��KClO3��3H2O���ݴ˷������ۣ�
A�������п��ܺ���KCl��KClO��KClO3������������K��Cl��ԭ�Ӹ����Ⱦ�Ϊ1��1������˲μӷ�Ӧ��KOH��Cl2֮��Ϊ2��1�����μӷ�Ӧ���������ʵ���Ϊ![]() mol����A˵����ȷ��
mol����A˵����ȷ��
B����ֻ����3Cl2��6KOH=5KCl��KClO3��3H2Oʱ��KClO3�IJ������n(KClO3)= ![]() mol����B˵������
mol����B˵������
C����ֻ����Cl2��2KOH=KCl��KClO��H2O����ת�Ƶ������ʵ���Ϊ![]() mol����ֻ����3Cl2��6KOH=5KCl��KClO3��3H2O����ת�Ƶ������ʵ���Ϊ
mol����ֻ����3Cl2��6KOH=5KCl��KClO3��3H2O����ת�Ƶ������ʵ���Ϊ![]() mol����˷�Ӧ��ת�Ƶ��ӵ����ʵ�����Χ��
mol����˷�Ӧ��ת�Ƶ��ӵ����ʵ�����Χ��![]() mol��n(e��)��
mol��n(e��)��![]() mol����C˵����ȷ��
mol����C˵����ȷ��
D������n(Cl��)=11mol����n(ClO��)=1mol�����ݵ�ʧ������Ŀ�غ㣬11mol=1mol��n(ClO3��)��5���ó�n(ClO3��)=2mol�������![]() =
=![]() ����D˵����ȷ��
����D˵����ȷ��
��ΪB��

 ������������Ծ�ϵ�д�
������������Ծ�ϵ�д� �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д�����Ŀ��POCl3�������뵼����Ӽ������άԭ�ϣ�ʵ�����Ʊ�POCl3���ⶨ��Ʒ������ʵ��������£�
I���Ʊ�PCl3
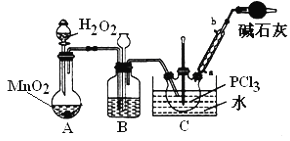
��1��ʵ�����ø�����غ�Ũ���ᷴӦ������������װ�ÿ�����ͼ�е�____������ĸ���ţ���
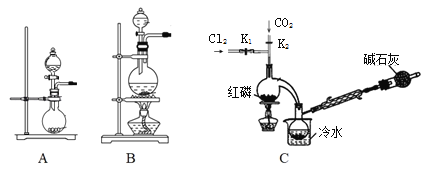
��2�����װ��C�����Բ�װ��ҩƷ���ȹر�K1����K2ͨ������CO2��һ��ʱ��ر�K2����������ƿͬʱ��K1ͨ�������������Ӧ�������С�ͼ�м�ʯ�ҵ�������______________��
II��ʵ�����Ʊ�POCl3��
������������Һ̬PCl3����ȡPOCl3��ʵ��װ�ã����ȼ��г������ԣ���ͼ��
���ϣ���Ag++SCN����AgSCN����Ksp��AgCl����Ksp��AgSCN����
��PCl3��POCl3�������Ϣ���±���
���� | �۵�/�� | �е�/�� | ��Է������� | ���� |
PCl3 | ��112.0 | 76.0 | 137.5 | �����ܣ���Ϊ��ɫҺ�壬��ˮ�����ҷ�Ӧ���ɺ�������Ȼ��� |
POCl3 | 2.0 | 106.0 | 153.5 |
��3��POCl3�ڳ�ʪ�����л���ҡ����̡�����Ӧ�Ļ�ѧ����ʽΪ___________________________________��
��4����Ӧ�¶�Ҫ������60��65�棬ԭ���ǣ�_________________________________��
��5��ͨ��������·����Բⶨ��Ʒ��ClԪ�غ�����ʵ�鲽�����£�
a��ȷ��ȡ15.0 g POCl3��Ʒ������ʢ��60.00 mL����ˮ��ˮ��ƿ��ҡ������ȫˮ�⣬��ˮ��Һ���100.00 mL��Һ��
b��ȡ10.00 mL��Һ����ƿ�У�����10.00 mL 3.2 molL��1 AgNO3����Һ��
c��������������������ҡ����ʹ�������汻�л��︲�ǡ�
d����NH4Fe (SO4) 2Ϊָʾ������0.2 molL��1 NH4SCN��Һ�ζ�������AgNO3��Һ���ﵽ�ζ��յ�ʱ����ȥl0.00 mL NH4SCN��Һ��
�ٲ���d�дﵽ�ζ��յ��������__________________________________________��
�ڲ�Ʒ��ClԪ�ص���������Ϊ______________������3λ��Ч���֣���
����Ŀ���±�ΪԪ�����ڱ���һ���֡�
̼ | �� | Y | |
X | �� | Z |
�ش��������⣺
��1������Ԫ��ԭ�Ӱ뾶�����ǣ�дԪ�ط��ţ�___��Yԭ�ӵĵ����Ų�ʽ��__��Zԭ�Ӻ������������ߵĵ����Dz���___��
��2��������ʵ��˵��YԪ�صķǽ����Ա�SԪ��ǿ����___��
a.Y������H2S��Һ��Ӧ����Һ�����
b.��������ԭ��Ӧ�У�1mol Y���ʱ�1mol S�õ��Ӷ�
c.Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��3��CCl4��һ�ֳ������л��ܼ���д�������ʽ___���ж������ں���___������ԡ������Ǽ��ԡ������ۼ���____���ӣ�����ԡ��Ǽ��ԡ�����SiH4�ķе��CH4�ߣ�ԭ����___��
��4��̼������Һ�е����̪����Һ�Ժ�ɫ���������ӷ���ʽ˵�������������ԭ��___����������ɫ����Һ�м��������Ȼ��ƹ��壬��Һ��ɫ��dz������ƽ�����۽��Ͳ����������ԭ��____��