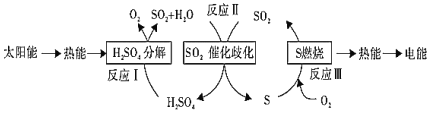
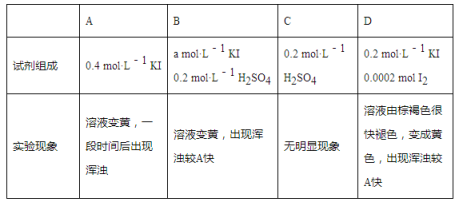
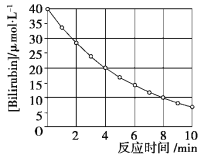
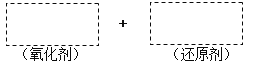��Ŀ����
����Ŀ��POCl3�������뵼����Ӽ������άԭ�ϣ�ʵ�����Ʊ�POCl3���ⶨ��Ʒ������ʵ��������£�
I���Ʊ�PCl3
��1��ʵ�����ø�����غ�Ũ���ᷴӦ������������װ�ÿ�����ͼ�е�____������ĸ���ţ���
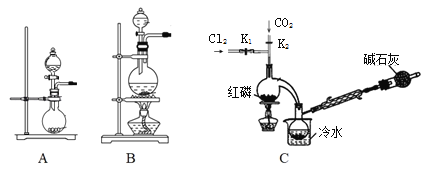
��2�����װ��C�����Բ�װ��ҩƷ���ȹر�K1����K2ͨ������CO2��һ��ʱ��ر�K2����������ƿͬʱ��K1ͨ�������������Ӧ�������С�ͼ�м�ʯ�ҵ�������______________��
II��ʵ�����Ʊ�POCl3��
������������Һ̬PCl3����ȡPOCl3��ʵ��װ�ã����ȼ��г������ԣ���ͼ��
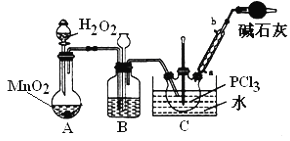
���ϣ���Ag++SCN����AgSCN����Ksp��AgCl����Ksp��AgSCN����
��PCl3��POCl3�������Ϣ���±���
���� | �۵�/�� | �е�/�� | ��Է������� | ���� |
PCl3 | ��112.0 | 76.0 | 137.5 | �����ܣ���Ϊ��ɫҺ�壬��ˮ�����ҷ�Ӧ���ɺ�������Ȼ��� |
POCl3 | 2.0 | 106.0 | 153.5 |
��3��POCl3�ڳ�ʪ�����л���ҡ����̡�����Ӧ�Ļ�ѧ����ʽΪ___________________________________��
��4����Ӧ�¶�Ҫ������60��65�棬ԭ���ǣ�_________________________________��
��5��ͨ��������·����Բⶨ��Ʒ��ClԪ�غ�����ʵ�鲽�����£�
a��ȷ��ȡ15.0 g POCl3��Ʒ������ʢ��60.00 mL����ˮ��ˮ��ƿ��ҡ������ȫˮ�⣬��ˮ��Һ���100.00 mL��Һ��
b��ȡ10.00 mL��Һ����ƿ�У�����10.00 mL 3.2 molL��1 AgNO3����Һ��
c��������������������ҡ����ʹ�������汻�л��︲�ǡ�
d����NH4Fe (SO4) 2Ϊָʾ������0.2 molL��1 NH4SCN��Һ�ζ�������AgNO3��Һ���ﵽ�ζ��յ�ʱ����ȥl0.00 mL NH4SCN��Һ��
�ٲ���d�дﵽ�ζ��յ��������__________________________________________��
�ڲ�Ʒ��ClԪ�ص���������Ϊ______________������3λ��Ч���֣���
���𰸡�A ����β��������ֹ�����е�ˮ��������������ƿ POCl3+3H2O��H3PO4+3HCl �¶ȹ��ͣ���Ӧ�ٶ�̫�����¶ȹ��ߣ�PCl3�ӷ��������ʵ� ��Һ����ɫ��Ϊ��ɫ��30 s�ڲ��ٱ�ɫ 71.0%
��������
I����1��������غ�Ũ���ᷴӦ�����������ڹ����Һ�巴Ӧ����Ӧ����Ҫ���ȣ��ݴ�ѡ��װ�ã�
��2�����������ж�����ƷPCl3��ˮ�����ҷ�Ӧ���ɺ�������Ȼ�����з�����
II��ʵ�����Ʊ�POCl3��Aװ������˫��ˮ��������̷�Ӧ����������ͨ������˫��ˮ���������Կ��Ʋ������������ʣ������к���ˮ������Ũ�����ȥ������Bװ����װŨ���ᣬװ��B���г���©��������ƽ��װ�������ѹǿ����ȫƿ�����ã����������������Ȼ���Ӧ����POCl3��Ϊ�˿��Ʒ�Ӧ������Ҫ��ֹ���Ȼ��ӷ�����Ӧ���¶ȿ�����60��65��������װ��C����ˮԡ��Ϊ��ֹPOCl3�ӷ����������ܽ�������������POCl3��ˮ������ˮ��Ϊ��������Ȼ��⣬����Ϊ��ֹ������ˮ��������װ�ã�ͬʱ����β����������װ�õ�������м�ʯ�ҵĸ���ܣ��ݴ˷����ش����⡣
I����1�������Һ�巴Ӧ����Ӧ����Ҫ���ȣ��ݴ�ѡ��װ��A��
�𰸣�A��
��2�����������ж������β�������ŷŵ������У���ƷPCl3��ˮ���ҷ�Ӧ��Ҫ��ֹ�����е�ˮ��������������ƿ��
�𰸣�����β��������ֹ�����е�ˮ��������������ƿ��
II����3��POCl3�ڳ�ʪ�����л��������������ȷ����HCl���ɣ�������Ԫ�صĻ��ϼۻ�����ȷ�����������ɣ�����ʽΪPOCl3+3H2O��H3PO4+3HCl��
�𰸣�POCl3+3H2O��H3PO4+3HCl ��
��4����������ķ�����֪����Ӧ�¶�Ӧ������60��65����ԭ�����¶ȹ��ͣ���Ӧ����С���¶ȹ��ߣ����Ȼ���ӷ��������ʵͣ�
�𰸣��¶ȹ��ͣ���Ӧ�ٶ�̫�����¶ȹ��ߣ�PCl3�ӷ��������ʵ� ��
��5����ΪFe3+��SCN-��ϣ���Һ���죬�����NH4Fe (SO4) 2Ϊָʾ������0.2 molL��1 NH4SCN��Һ�ζ�������AgNO3��Һ���ﵽ�ζ��յ����������Һ����ɫ��Ϊ��ɫ��30 s�ڲ��ٱ�ɫ��
�𰸣���Һ����ɫ��Ϊ��ɫ��30 s�ڲ��ٱ�ɫ��
��6���ⶨPOCl3��Ʒ��������POCl3��ˮ��Ӧ�����Ȼ��⣬Ȼ��������������Һ������Һ�е������ӣ�NH4SCN��Һ�ζ�������AgNO3��Һ������NH4SCN�����ʵ����ɼ������Һ��ʣ���AgNO3�����AgNO3�������ʵ�����֪�������ӷ�Ӧ���������������������Һ�������ӵ����ʵ���������ȷ����Ԫ�ص�����������NH4SCN�����ʵ���Ϊ0.2mol/L��0.01L=0.002mol�����ݷ�ӦAg++SCN-=AgSCN������֪��Һ��ʣ��������ӵ����ʵ���Ϊ0.002mol��POCl3��ˮ��Ӧ�����Ȼ�������ʵ���Ϊ��3.2��0.01mol-0.002mol����10=0.3mol����Ԫ�ص���������Ϊ![]() ��100%=71.0%��
��100%=71.0%��
�𰸣�71.0%��