��Ŀ����
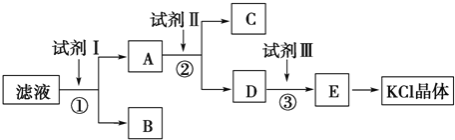
����Ŀ��AԪ�ص�һ�ֵ�������Ҫ�İ뵼����ϣ���AԪ�ص�һ�ֻ�����C��������������ܵ��ִ�ͨѶ���������ά��C���ռӦ���ɺ�AԪ�صĻ�����D��
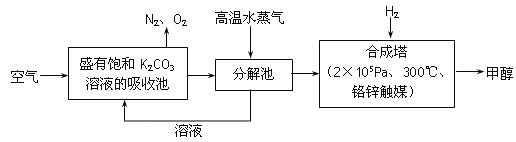
(1)����C������ѧ��Ӧ������________����Ӧ�Ļ�ѧ����ʽ��_______________ ��
(2)��C�봿���ϣ��ڸ�������ʱ������ѧ��ӦҲ������D��ͬʱ������B�����������E����E��D��������ˮ�л�Ϻ��ַ�����ѧ��Ӧ���ɺ�A�Ļ�����F��
��д������D��F�Ļ�ѧ��Ӧ����ʽ��____________________��__________________��
��Ҫ�������ڸ������ۻ������������в���ѡ�õ���________��
A����ͨ�������� B��ʯӢ�������� C�������� D��������
���𰸡������ SiO2��4HF=SiF4����2H2O SiO2��Na2CO3![]() Na2SiO3��CO2�� Na2SiO3��CO2��H2O=Na2CO3��H2SiO3�� ABC
Na2SiO3��CO2�� Na2SiO3��CO2��H2O=Na2CO3��H2SiO3�� ABC
��������
��AԪ�ص�һ�ֵ�������Ҫ�İ뵼�������˵��AΪSi��ͨ�������ά�����Ʋ�CΪSiO2��SiO2���ռ�������Ʒ�Ӧ���ɵĺ�SiԪ�صĻ�����ΪNa2 SiO3��SiO2�봿�̼���Ƹ�������������Na2 SiO3��CO2����BΪC��EΪCO2��������̼������������ˮ�п����ɹ����̼���ƣ���FΪH2SiO3��
��1��SiO2��������ᷢ����Ӧ���ʴ�Ϊ������![]() ��
��
��2���ٸ��ݷ�����֪��Ϊ��![]() ��
��![]() ��
��
��A����ͨ���������к���SiO2�����ڸ������봿�Ӧ����A�����B��ʯӢ���������к���SiO2�����ڸ������봿�Ӧ����B�����C��������к���SiO2�����ڸ������봿�Ӧ����C�����D���������в��������������봿�Ӧ�����ʣ���D����ȷ���ʴ�Ϊ��ABC��

����Ŀ�������Ѱ۳����ᣨ��Ҫ�����ᡢFe3+��Fe2+��TiO2+��Al3+���Ʊ����������[(NH4)2S2O8]��ͬʱ����TiO(OH)2�ļ�Ҫ�������£�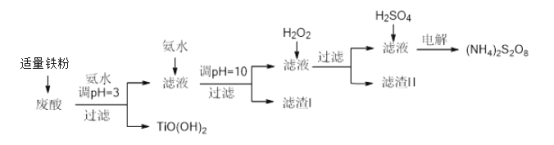
��֪��i.����������ȫ�����������������pH��
�������� | TiO2+ | Fe3+ | Fe2+ | Al3+ |
��ʼ������PH | 1.2 | 1.9 | 7.0 | 3.2 |
������ȫ��pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7ʱ��Fe2+��������Fe(II)��������[Fe(NH3)2]2+��
��ش��������⣺
��1��������������������______________________________________��
��2������TiO(OH)2�Ļ�ѧ����ʽ��________________________________��
��3������I���������о����е����ʵĻ�ѧʽ��___________________________��
��4������H2O2��Ŀ������������Fe(II)��������[Fe(NH3)2]2+����ƽ�������ӷ���ʽ��
2[Fe(NH3)2]2+ +____________+4H2O +H2O2 =___________ + 4NH3��H2O ��
��5�������£����Һ�к�������Ҫ������ʽ��pH�Ĺ�ϵ����ͼ��ʾ��
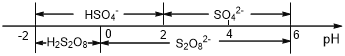
�������ŵ��������ҪΪHSO4-���������������Һ��pH��ΧΪ___________________________________
��6����֪Ksp[Al(OH)3]=3.2��10-34 ����pH=10 ʱ������Һ��c(Al3+)=______________
��7��25�棬pH=3��(NH4)2SO4��Һ�У�����2c(SO42-)- c(NH4+) =_______mol/L����ʽ���ɣ���
����Ŀ���������л��ϳ��г��õ��ܼ���ijʵ��С����ʵ���������Ҵ���ˮ�Ʊ����ѣ�װ��ʾ��ͼ���гֺͼ���װ������ȥ�����й����ݺ�ʵ�鲽�����£�
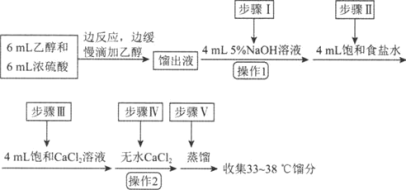
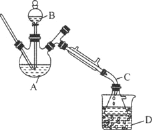
���� | ��Է������� | �ܶȣ���g��mL��1�� | �е㣯�� | ��ˮ�е��ܽ��� |
�Ҵ� | 46 | 0.816 | 78 | ���� |
���� | 74 | 0.713 | 34.6 | ���� |
��֪������ͬ�����£������ڱ���ʳ��ˮ�б���ˮ�и����ܡ�
���Ȼ��ƿ����Ҵ��γ������CaCl2��6C2H5OH��
��ش��������⣺
��1������B������Ϊ________��
��2�����Ҵ��Ʊ����ѵ��ܷ�ӦΪ2C2H5OH![]() CH3CH2OCH2CH3��H2O���˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH��H2SO4
CH3CH2OCH2CH3��H2O���˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH��H2SO4![]() CH3CH2OSO2OH��H2O����ڶ�����Ӧ�Ļ�ѧ����ʽΪ________��
CH3CH2OSO2OH��H2O����ڶ�����Ӧ�Ļ�ѧ����ʽΪ________��
��3����Ӧ�����У�����B��ĩ��Ӧ���뷴ӦҺ�У�ԭ����________________��
��4������D��ʢ�б�ˮ����������Ϊ________________��
��5������1������Ϊ________������2������Ϊ________��
��6����ʡ�Բ������ᵼ�µĺ����________��