题目内容
室温下,下列溶液中c(H+)最小的是( )
| A、c(OH-)=1×10-11mol?L-1 |
| B、pH=3的CH3COOH溶液 |
| C、pH=4的H2SO4溶液 |
| D、c(H+)=1×10-3mol?L-1 |
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:常温下水的离子积为1×10-14,若已知溶液的pH,可以直接根据c(H+)=10-pHmol?L-1计算出溶液中氢离子浓度,若告诉的是溶液中氢氧根离子浓度,则根据c(H+)=
mol/L计算出溶液中氢离子浓度,据此对各选项进行计算,然后找出溶液中c(H+)最小的选项.
| 1×10-14 |
| c(OH-) |
解答:
解:A.c(OH-)=1×10-11mol?L-1,则溶液中c(H+)=
mol/L=
mol/L=1×10-3mol?L-1;
B.pH=3的CH3COOH溶液中,c(H+)=10-pHmol?L-1=1×10-3mol?L-1;
C.pH=4的H2SO4溶液中,c(H+)=10-pHmol?L-1=1×104mol?L-1;
D.c(H+)=1×10-3mol?L-1;
根据以上分析可知,溶液中氢离子浓度最小的是C,
故选C.
| 1×10-14 |
| c(OH-) |
| 1×10-14 |
| 1×10-11 |
B.pH=3的CH3COOH溶液中,c(H+)=10-pHmol?L-1=1×10-3mol?L-1;
C.pH=4的H2SO4溶液中,c(H+)=10-pHmol?L-1=1×104mol?L-1;
D.c(H+)=1×10-3mol?L-1;
根据以上分析可知,溶液中氢离子浓度最小的是C,
故选C.
点评:本题考查了有关pH的简单计算,题目难度不大,注意掌握溶液酸碱性与溶液pH的关系,能够根据溶液pH、溶液中氢氧根离子浓度计算出氢离子浓度.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
下列实验中,仪器的下端必须插入液面下的是( )
①制备氢气的简易装置中的长颈漏斗;
②制备氯气时发生装置中的分液漏斗;
③制备硝基苯时的温度计;
④用乙醇制取乙烯时的温度计;
⑤分馏石油时的温度计.
①制备氢气的简易装置中的长颈漏斗;
②制备氯气时发生装置中的分液漏斗;
③制备硝基苯时的温度计;
④用乙醇制取乙烯时的温度计;
⑤分馏石油时的温度计.
| A、①③④ | B、②④⑤ |
| C、③④⑤ | D、全部 |
下列说法正确的是( )
| A、常温下,20L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA | ||
| B、中和等体积、等物质的量浓度盐酸和醋酸溶液,盐酸所需NaOH溶液多于醋酸 | ||
C、向0.1mol/L NH3?H2O溶液中加入少量NH4Cl固 体,溶液中
| ||
| D、一定温度下,10mL 0.50mol?L-1 NH4Cl溶液与20mL 0.25mol?L-1 NH4Cl溶液含NH4+物质的量相同 |
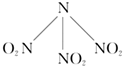 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )| A、该分子是既含有极性键又含有非极性键的非极性分子 |
| B、该物质就是N2O3 |
| C、分子中四个氮原子共平面 |
| D、该物质既有氧化性又有还原性 |
某化学实验报告中有如下记录,其中实验数据合理的是( )
| A、用25mL酸式滴定管量取5.6mL的稀硝酸 |
| B、用广泛的pH试纸测得溶液的pH为6.2 |
| C、温度计显示的室温读数为25.69℃ |
| D、用托盘天平称取11.7g CuO粉末 |
0.1mol的某烃充分燃烧生成4.48L的CO2(标况),则该烃可能是( )
| A、CH4 |
| B、C2H6 |
| C、C4H8 |
| D、C6H6 |
下列说法正确的是( )
| A、碘化铵和氯化铵受热分解过程中破坏和形成的化学键类型完全相同 |
| B、反应N2H4(I)═N2(g)+2H2(g)是一个△S>0的反应 |
| C、40g金刚砂(SiC)中含有C-Si键的个数为2NA(NA为阿伏加德罗常数) |
| D、HClO是弱酸,所以NaClO是弱电解质 |
下列有关离子的检验方法一定正确的是( )
| A、向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含Ag+ |
| B、向某溶液中滴加KSCN溶液无明显现象,再滴入新制的氯水,溶液出现血红色则说明原溶液中含Fe2+ |
| C、向某溶液中滴加足量稀HCl,产生气体使澄清石灰水变浑浊,则说明原溶液中一定含CO32- |
| D、用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色,说明原溶液中不含K+ |