题目内容
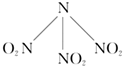 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )| A、该分子是既含有极性键又含有非极性键的非极性分子 |
| B、该物质就是N2O3 |
| C、分子中四个氮原子共平面 |
| D、该物质既有氧化性又有还原性 |
考点:物质的组成、结构和性质的关系,不同晶体的结构微粒及微粒间作用力的区别
专题:元素及其化合物
分析:A.根据信息中该分子中N-N-N键角都是108.1°及N(NO2)3的结构应与氨气相似可知该分子为三角锥形结构,正负电荷中心不重合;
B.三氧化二氮的结构简式为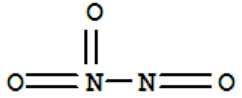 ,据此判断;
,据此判断;
C.根据信息中该分子中N-N-N键角都是108.1°及N(NO2)3的结构应与氨气相似,则分子中四个氮原子不共平面;
D.依据元素的化合价来分析其性质.
B.三氧化二氮的结构简式为
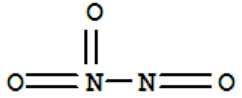 ,据此判断;
,据此判断;C.根据信息中该分子中N-N-N键角都是108.1°及N(NO2)3的结构应与氨气相似,则分子中四个氮原子不共平面;
D.依据元素的化合价来分析其性质.
解答:
解:A.该分子是既含有N-O极性键又含有N-N非极性键,但是其正负电荷中心不重合,属于极性分子,故A错误;
B.三氧化二氮与N(NO2)3结构不同,不是同种物质,故B错误;
C.该分子中N-N-N键角都是108.1°,推知分子中4个氮原子在空间呈四面体型,所以分子中四个氧原子不可能共平面,故C错误;
D.该分子中的氮既有+3价也有+5价,+3价氮处于中间价态,既有氧化性又有还原性,故D正确;
故选:D.
B.三氧化二氮与N(NO2)3结构不同,不是同种物质,故B错误;
C.该分子中N-N-N键角都是108.1°,推知分子中4个氮原子在空间呈四面体型,所以分子中四个氧原子不可能共平面,故C错误;
D.该分子中的氮既有+3价也有+5价,+3价氮处于中间价态,既有氧化性又有还原性,故D正确;
故选:D.
点评:本题为通过给出信息,考查了物质的结构和性质,题目难度中等,熟悉氨气分子的模型是解题的关键,注意知识的迁移应用.

练习册系列答案
相关题目
25℃时,下列各溶液中[H+]最小的是( )
| A、C(H+)=1×10-5mol/L |
| B、pH=8的溶液 |
| C、稀释1mL 1mol/L NaOH溶液到1L后所得溶液 |
| D、0.11mol/L NaOH溶液跟等体积0.05mol/L H2SO4溶液的混合液 |
下列关于乙炔制取的说法不正确的是( )
| A、为了加快反应速率可用饱和食盐水代替水反应 |
| B、此反应是放热反应 |
| C、为了除去杂质气体,除了用硫酸铜外还可用氢氧化钠溶液 |
| D、反应中不需加碎瓷片作沸石 |
pH=9的氢氧化钠和醋酸钠两种溶液中,设由水电离产生的[OH-]为A mol?L-1和B mol?L-1则A与B的关系是( )
| A、A=10-4B |
| B、A>B |
| C、B=10-4A |
| D、A=B |
室温下,下列溶液中c(H+)最小的是( )
| A、c(OH-)=1×10-11mol?L-1 |
| B、pH=3的CH3COOH溶液 |
| C、pH=4的H2SO4溶液 |
| D、c(H+)=1×10-3mol?L-1 |
以下各项的比值是2:1的是( )
| A、CuCl2溶液中Cl-与Cu2+的物质的量浓度之比 |
| B、pH均为2的盐酸和硫酸的物质的量 |
| C、同温下0.2mol/L的醋酸和0.1mol/L的醋酸中c(H+) |
| D、同浓度的NaOH与Ba(OH)2中和等物质的量的HCl所消耗的碱的体积 |
下列实验无法达到下列目的是( )
| A、用升华法分离碘和NaCl的混合物 |
| B、用结晶法分离KNO3和NaCl的混合物 |
| C、用分液法分离水和汽油的混合物 |
| D、用蒸馏法分离乙醇(沸点为78℃)和乙酸乙酯(沸点为77.5℃)的混合物 |
下列离子方程式,正确的是( )
| A、澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2═CaCO3↓+H2O |
| B、碳酸钠溶液中加入二氧化硅:CO32-+SiO2═SiO32-+CO2↑ |
| C、二氧化硅与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O↑ |
| D、硅酸与烧碱溶液中和:H2SiO3+2OH-═SiO32-+2H2O |
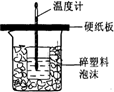 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题: