题目内容
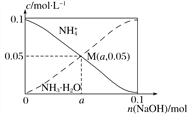
【题目】“创新”化学小组对某Na2CO3和NaHCO3的混合溶液(以下简称“样品溶液”)的组成进行探究,取20.0mL样品溶液,向其中逐滴滴入0.10molL﹣1的稀盐酸,边滴边振荡,滴入盐酸的体积和产生的现象见下表.
反应阶段 | Ⅰ | Ⅱ | Ⅲ |
盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
现象 | 无气体 | 产生气体 | 无气体 |
请回答下列问题:
(1)配制0.10molL﹣1的稀盐酸250mL,需要10.0molL﹣1的浓盐酸的体积为mL.
(2)计算样品溶液中碳酸根离子的物质的量浓度.
【答案】
(1)2.5
(2)当加入10mL稀盐酸时,恰好把样品中的碳酸根离子完全转化为碳酸氢根离子,10mL稀盐酸的物质的量为0.010L×0.10mol/L=0.001mol;
设20.0mL样品溶液中碳酸根离子的物质的量为y则:
CO ![]() +H+HCO
+H+HCO ![]()
1 1
y 0.001mol
解得y=0.001mol,则样品中碳酸根离子物质的量浓度C= ![]() =0.05mol/L;
=0.05mol/L;
故答案为:0.05mol/L
【解析】解:(1)配制0.10molL﹣1的稀盐酸250mL设需要浓盐酸的体积为V,则依据溶液稀释过程中所含溶质的物质的量不变得:V×10.0mol/L=0.10mol/L×250mL,解得V=2.5mL;所以答案是:2.5mL;

练习册系列答案
相关题目