题目内容
【题目】常用药——羟苯水杨胺,其合成路线如下。回答下列问题:

(1)羟苯水杨胺的化学式为 。1 mol羟苯水杨胺最多可以和 ____ mol NaOH反应。
(2)D中官能团的名称 。
(3)A→B反应所加的试剂是 。
(4)F在一定条件下发生缩聚反应的化学方程式为 。
(5) F存在多种同分异构体。F的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是 。
A.质谱仪 B.红外光谱仪 C.元素分析仪 D.核磁共振仪
(6)F的同分异构体中既能与FeCl3发生显色反应,又能发生银镜反应,且核磁共振氢谱显示4组峰,峰面积之比为1:2:2:1的同分异构体的结构简式(任写一种即可) 。
【答案】
(1)C13H11NO3;3;
(2)硝基、羟基
(3)浓硫酸和浓硝酸
(4)
(5) C;
(6)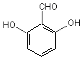 、
、 、
、  (任写其一)
(任写其一)
【解析】
试题分析:由羟苯水杨胺结构简式、F的分子式可知,F为![]() ,E为
,E为![]() ,由反应信息逆推可知D为
,由反应信息逆推可知D为![]() ,由转化关系可知,苯与氯气发生取代反应生成A为
,由转化关系可知,苯与氯气发生取代反应生成A为![]() ,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为
,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为![]() ,B发生水解反应生成C为
,B发生水解反应生成C为![]() ,C酸化得到D。
,C酸化得到D。
(1)由羟苯水杨胺的结构简式,可知其化学式为C13H11NO3,1mol羟苯水杨胺含有2mol酚羟基,水解得到1mol-COOH,最多可以和3mol NaOH反应,故答案为:C13H11NO3;3;
(2)D为![]() ,含有官能团由羟基、硝基,故答案为:羟基、硝基;
,含有官能团由羟基、硝基,故答案为:羟基、硝基;
(3)A→B所需试剂为:浓硝酸和浓硫酸,故答案为:浓硝酸和浓硫酸;
(4)F在一定条件下发生缩聚反应的化学方程式为: ,故答案为:
,故答案为: ;
;
(5)F及同分异构体中组成元素相同,结构不同,由元素分析仪显示的信号(或数据)完全相同,故选:C;
(6)F(![]() )的同分异构体中既能与FeCl3发生显色反应,又能发生银镜反应,说明含有酚羟基、醛基,侧链为-OH、-OOCH时,有邻、间、对3种,侧链可为-CHO、2个-OH,2个-OH处于邻位,-CHO有2种位置,2个-OH处于间位,-CHO有3种位置,2个-OH处于对位,-CHO有1种位置,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:2:1的同分异构体的结构简式为:
)的同分异构体中既能与FeCl3发生显色反应,又能发生银镜反应,说明含有酚羟基、醛基,侧链为-OH、-OOCH时,有邻、间、对3种,侧链可为-CHO、2个-OH,2个-OH处于邻位,-CHO有2种位置,2个-OH处于间位,-CHO有3种位置,2个-OH处于对位,-CHO有1种位置,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:2:1的同分异构体的结构简式为: 、
、 、
、 ,故答案为:
,故答案为: 、
、 、
、 。
。

【题目】用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如下:
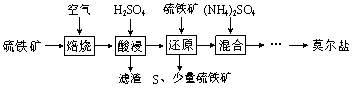
已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
2Fe3++ FeS2=2S↓+3Fe2+
(1)“还原”时,pH不宜过高的原因是_________,写出“还原”时反应Ⅱ的离子方程式:__________。
(2)实验测得“还原”时反应Ⅰ、Ⅱ中被还原的Fe3+的物质的量之比为2:7。计算“还原”后溶液Fe2+的浓度即可确定后面所加(NH4)2SO4的量(溶液体积变化忽略不计)
离子 | 离子浓度(mol·L-1) | |
还原前 | 还原后 | |
SO42- | 3.20 | 3.50 |
Fe2+ | 0.15 | |
(3)称取23.52g新制莫尔盐,溶于水配成溶液并分成两等份。一份加入足量的BaCl2溶液,得到白色沉淀13.98g;另一份用0.2000mol/LK2Cr2O7酸性溶液滴定,当Cr2O72-恰好完全被还原为Cr3+时,消耗溶液的体积为25.00mL。试确定莫尔盐的化学式(请给出计算过程)。