题目内容
【题目】2019年10月9日,瑞典皇家科学院在斯德哥尔摩宣布,将2019年诺贝尔化学奖颁发给来自美国、英国、日本的三位科学家,表彰他们在锂离子电池方面的研究贡献。高度评价他们“创造了一个可充电的世界”。锂离子电池与传统电池相比,充电更快,功率密度更高,使用时间更长,在手机和笔记本电脑等便携式电子产品上广泛应用。工业上常以锂辉矿(主要成分为 LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂,其中一种工艺流程如下:

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:

②Li2CO3的溶解度随温度变化如图所示:
试回答下列问题:
(1)酸浸时,为了提高浸取率可采取升高温度、粉碎矿石、搅拌、过滤后再次浸取等措施还可通过_______来提高浸取率。
(2)反应I中应调节pH范围为_______,沉淀A的成分除H2SiO3、CaCO3、Al(OH)3外,还有___________。
(3)反应Ⅱ的离子方程式为_________________。
(4)“操作I"的名称为______;洗涤Li2CO3沉淀要使用_______ (选填“热水”或“冷水”),理由是___________________________________________________。
【答案】延长浸取时间(或:增大酸的浓度) 4.7~9.6(或4.7≤ pH < 9.6) Fe(OH)3、CaSO4 Mg2++Ca(OH)2=Ca2++Mg(OH)2↓ (或:Mg2++2OH-=Mg(OH)2↓) CO32-+Ca(OH)2=CaCO3↓+2OH-(或:Ca2++CO32-= CaCO3↓) 过滤 热水 碳酸锂的溶解度随温度升高而降低,热水洗涤可以减少碳酸锂的溶解损失
【解析】
锂辉矿(主要成分为 LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂,加入过量硫酸溶解锂辉矿,再加入碳酸钙调节溶液的pH,加入双氧水将溶液里的亚铁离子氧化为铁离子,使铁离子和铝离子沉淀完全,过滤除去沉淀,然后加入氢氧化钙和碳酸钠除去溶液中的钙离子和镁离子,过滤得到的溶液中主要是锂离子的水溶液,蒸发浓缩,加入饱和的碳酸钠溶液沉淀锂离子生成碳酸锂,洗涤后加入盐酸溶解得到氯化锂溶液,加热蒸干得到氯化锂,电解氯化锂得到金属锂。根据以上分析解答此题。
(1)增大酸的浓度、升高温度、增大固体表面积、搅拌或延长浸取时间可以提高浸取率,所以为了提高浸取率可采取升高温度、粉碎矿石、搅拌、过滤后再次浸取等措施还可通过延长浸取时间或增大酸的浓度来提高浸取率;
答案为:延长浸取时间(或:增大酸的浓度)。
(2)反应Ⅰ中调节pH的目的是除去Fe3+、Al3+,由表中数据可知调节pH范围为4.7~9.6(或4.7≤pH<9.6),硫酸钙微溶于水,所以沉淀A的成分除H2SiO3、CaCO3、Al(OH)3外,还有Fe(OH)3、CaSO4 ;
答案为:4.7~9.6(或4.7≤pH<9.6);Fe(OH)3、CaSO4。
(3)反应Ⅱ调节pH=11,目的是除去Mg2+和Ca2+,根据加入的试剂,主要离子方程式为:Mg2++Ca(OH)2= Ca2++ Mg(OH)2↓(或:Mg2++2OH-=Mg(OH)2↓)、CO32-+ Ca(OH)2=CaCO3↓+2OH-(或:CO32-+ Ca2+=CaCO3↓);
答案为:Mg2++Ca(OH)2= Ca2++ Mg(OH)2↓(或:Mg2++2OH-=Mg(OH)2↓)、CO32-+ Ca(OH)2=CaCO3↓+2OH-(或:CO32-+ Ca2+=CaCO3↓)。
(4)“操作Ⅰ”目的是分离出固体碳酸锂,所以“操作Ⅰ”是过滤;由图可知碳酸锂的溶解度随温度升高而降低,热水洗涤可以减少碳酸锂的溶解损失,所以洗涤碳酸锂沉淀要用热水;
答案为:过滤;热水 ;碳酸锂的溶解度随温度升高而降低,热水洗涤可以减少碳酸锂的溶解损失。

 名校课堂系列答案
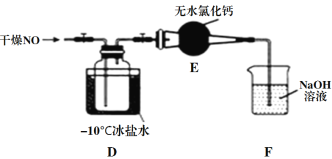
名校课堂系列答案【题目】某同学利用下图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )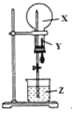
X气体 | Y试剂 | Z试剂 | |
A. | NO2 | H2O | H2O |
B. | CO2 | H2O | H2O |
C. | HCl | 饱和食盐水 | 水 |
D. | NO2 和O2 | H2O | H2O |
A.AB.BC.CD.D