ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩ(1)œ¬Ν–Ζ¥”Π τ”ΎΈϋ»»Ζ¥”ΠΒΡ «_________________________
ΔΌ¬ΝΖέ”κ―θΜ·ΧζΖέΡ©Ζ¥”Π ΔΎΥαΦν÷–ΚΆΖ¥”Π ΔέœθΥαοß»ή”ΎΥ° ΔήΧΦΥαΗΤΖ÷Ϋβ ΔίH2‘ΎCl2÷–»Φ…’ ΔόΉΤ»»ΒΡΧΦ”κCO2ΒΡΖ¥”Π ΔΏNH4ClΨßΧε”κBa(OH)28H2OΜλΚœΫΝΑη
(2)‘Ύ25ΓφΓΔ101kPaΒΡΧθΦΰœ¬Θ§ΕœΝ―1mol HΓΣHΦϋΈϋ ’436 kJΡήΝΩΘ§ΕœΝ―1 mol ClΓΣClΦϋΈϋ ’243 kJΡήΝΩΘ§–Έ≥…1mol HΓΣClΦϋΖ≈≥ω431 kJΡήΝΩΓΘΗΟΧθΦΰœ¬H2ΘΪCl2=2HClΖ¥”Π÷–ΒΡΡήΝΩ±δΜ·Ω…”Ο»γΆΦ±μ ΨΘΚ
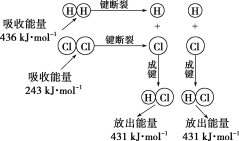
œ÷”–1 mol H2ΚΆ1 mol Cl2‘Ύ25ΓφΓΔ101 kPaœ¬Άξ»ΪΖ¥”ΠΓΘ«κΗυΨί…œ ω–≈œΔΜΊ¥πœ¬Ν–”–ΙΊΈ ΧβΘΚ
ΔΌΗΟΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ_____________
ΔΎΖ¥”ΠΈοΒΡΉήΡήΝΩ___________(ΧνΓΑΘΨΓ±ΜρΓΑΘΦΓ±)…ζ≥…ΈοΒΡΉήΡήΝΩΓΘ
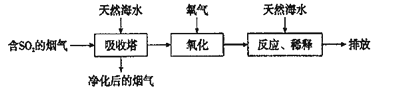
(3)÷±Ϋ”≈≈Ζ≈Κ§SO2ΒΡ―ΧΤχΜα–Έ≥…Υα”ξΘ§ΈΘΚΠΜΖΨ≥ΓΘΙΛ“Β…œ≥Θ≤…”Ο¥ΏΜ·ΜΙ‘≠Ζ®ΚΆΦνΈϋ ’Ζ®¥ΠάμSO2ΤχΧεΓΘ»γΆΦΥυ ΨΘΚ

1 mol CH4Άξ»Ϊ»Φ…’…ζ≥…ΤχΧ§Υ°ΒΡΡήΝΩ±δΜ·ΚΆ1 mol S(g)»Φ…’ΒΡΡήΝΩ±δΜ·ΓΘ‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬Θ§CH4Ω…“‘ΜΙ‘≠SO2…ζ≥…ΒΞ÷ S(g)ΓΔH2O(g)ΚΆCO2Θ§–¥≥ωΗΟΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ Ϋ____________ΓΘ
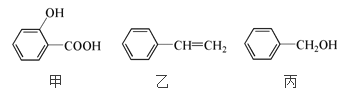
(4)ΦΗ÷÷Κ§Ιη‘ΣΥΊΒΡΈο÷ ÷°ΦδΒΡœύΜΞΉΣΜ·ΙΊœΒ»γΆΦΥυ ΨΘΚ
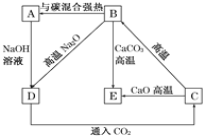
ΔΌ–¥≥ωœ¬Ν–Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
BΓζAΘΚ_________ΘΜ
BΓζEΘΚ_________ΓΘ
ΔΎ–¥≥ωœ¬Ν–»ή“Κ÷–Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚDΓζC_________ΓΘ
(5)Mg6Si4O10(OH)8”Ο―θΜ·ΈοΒΡ–Έ ΫΩ…±μ ΨΈΣ________ΓΘ
ΓΨ¥πΑΗΓΩΔήΔόΔΏ H2(g)ΘΪCl2(g)=2HCl(g) ΠΛH=Θ≠183 kJ/mol ΘΨ CH4(g)+2SO2(g)=2S(g)+CO2(g)+2H2O(g) H=+352 kJ/mol SiO2ΘΪ2C![]() SiΘΪ2COΓϋ CaCO3ΘΪSiO2
SiΘΪ2COΓϋ CaCO3ΘΪSiO2![]() CaSiO3ΘΪCO2Γϋ SiO32-ΘΪH2OΘΪCO2=H2SiO3ΓΐΘΪCO32- (ΜρSiO32-ΘΪ2H2OΘΪ2CO2=H2SiO3ΓΐΘΪ2HCO3-) 6MgO4SiO24H2O
CaSiO3ΘΪCO2Γϋ SiO32-ΘΪH2OΘΪCO2=H2SiO3ΓΐΘΪCO32- (ΜρSiO32-ΘΪ2H2OΘΪ2CO2=H2SiO3ΓΐΘΪ2HCO3-) 6MgO4SiO24H2O
ΓΨΫβΈωΓΩ
(1)ΗυΨί≥ΘΦϊΜ·―ßΖ¥”ΠΒΡ»»–ß”ΠΖ÷Έω≈–ΕœΘΜ
(2)ΔΌΗυΨίΖ¥”Π»»Β»”ΎΕœΝ―Ζ¥”ΠΈοΜ·―ßΦϋΈϋ ’ΒΡ»»ΝΩ”κ–Έ≥……ζ≥…ΈοΜ·―ßΦϋ ΆΖ≈ΒΡ»»ΝΩΒΡ≤νΦΤΥψΖ¥”Π»»Θ§≤Δ ι–¥»»Μ·―ßΖΫ≥Χ ΫΘΜ
ΔΎ»τΖ¥”ΠΈοΒΡΉήΡήΝΩ±»…ζ≥…ΈοΒΡΉήΡήΝΩΗΏΘ§‘ρΖ¥”ΠΈΣΖ≈»»Ζ¥”ΠΘ§Ζώ‘ρΈΣΈϋ»»Ζ¥”ΠΘΜ
(3)ΗυΨίΆΦ Ψœ»–¥≥ωCH4ΓΔS»Φ…’ΒΡ»»Μ·―ßΖΫ≥Χ ΫΘ§»ΜΚσΫΪΖΫ≥Χ ΫΒΰΦ”Θ§Ω…ΒΟ¥ΐ«σΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΜ
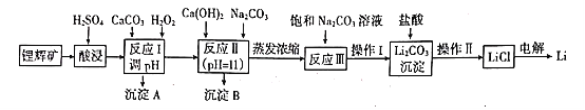
(4)“―÷ΣΦΗ÷÷Κ§Ιη‘ΣΥΊΒΡΈο÷ ÷°ΦδΒΡœύΜΞΉΣΜ·ΙΊœΒΘ§B”κΫΙΧΩΗΏΈ¬Ζ¥”Π≤ζ…ζAΘ§B”κNa2O‘ΎΗΏΈ¬œ¬“≤Ζ¥”Π≤ζ…ζDΘ§A”κNaOH»ή“ΚΖ¥”Π≤ζ…ζDΘ§ΫαΚœΈο÷ ΒΡ–‘÷ Ω…÷ΣΘΚBΈΣSiO2Θ§AΈΣSiΘ§DΈΣNa2SiO3Θ§B”κCaCO3ΗΏΈ¬Ζ¥”Π≤ζ…ζEΘ§‘ρE «CaSiO3Θ§CΗΏΈ¬«Ω»»Ζ¥”Π≤ζ…ζBΘ§C”κCaOΗΏΈ¬Ζ¥”Π≤ζ…ζCaSiO3Θ§«“œρNa2SiO3»ή“Κ÷–Ά®»κCO2ΤχΧεΘ§≤ζ…ζ≤ζ…ζCΘ§‘ρCΈΣH2SiO3Θ§»ΜΚσΫαΚœΈο÷ ΒΡ–‘÷ “‘ΦΑΧβΡΩ“Σ«σΫχ––Ϋβ¥πΓΘ
(5)ΙηΥα―Έ”Ο―θΜ·Έο–Έ Ϋ±μ Ψ ±Θ§œ»–¥Ϋπ τ―θΜ·ΈοΘ§‘Ό–¥Ζ«Ϋπ τ―θΜ·ΈοΘ§ΉνΚσ–¥Υ°Θ§Ης÷÷‘ΣΥΊΒΡ‘≠Ή”Ηω ΐ±»≤Μ±δΓΘ
(1)ΔΌ¬ΝΖέ”κ―θΜ·ΧζΖέΡ©Ζ¥”ΠΖ≈≥ω»»ΝΩΘ§ «Ζ≈»»Ζ¥”ΠΘΜ
ΔΎΥαΦν÷–ΚΆΖ¥”ΠΖ≈≥ω»»ΝΩΘ§ «Ζ≈»»Ζ¥”ΠΘΜ
ΔέœθΥαοß»ή”ΎΥ°Έϋ ’»»ΝΩΘ§Έο÷ »ήΫβΙΐ≥Χ «Έοάμ±δΜ·Θ§ΟΜ”–ΖΔ…ζΜ·―ßΖ¥”ΠΘΜ
ΔήΧΦΥαΗΤΖ÷ΫβΈϋ ’»»ΝΩΘ§ «Έϋ»»Ζ¥”ΠΘΜ
ΔίH2‘ΎCl2÷–»Φ…’Ζ≈≥ω»»ΝΩΘ§ «Ζ≈»»Ζ¥”ΠΘΜ
ΔόΉΤ»»ΒΡΧΦ”κCO2ΒΡΖ¥”ΠΈϋ ’»»ΝΩΘ§ «Έϋ»»Ζ¥”ΠΘΜ
ΔΏNH4ClΨßΧε”κBa(OH)28H2OΜλΚœΫΝΑηΈϋ ’»»ΝΩΘ§ «Έϋ»»Ζ¥”ΠΘΜ
Ήέ…œΥυ ωΩ…÷ΣΘΚ τ”ΎΈϋ»»Ζ¥”ΠΒΡΈΣΔήΔόΔΏΘΜ
(2)ΔΌΖ¥”Π»»Β»”ΎΕœΝ―Ζ¥”ΠΈοΜ·―ßΦϋΈϋ ’ΒΡ»»ΝΩ”κ–Έ≥……ζ≥…ΈοΜ·―ßΦϋ ΆΖ≈ΒΡ»»ΝΩΒΡ≤νΘ§‘Ύ25ΓφΓΔ101 kPaΒΡΧθΦΰœ¬Θ§ΕœΝ―1 mol H-HΦϋΈϋ ’436 kJΡήΝΩΘ§ΕœΝ―1 mol Cl-ClΦϋΈϋ ’243 kJΡήΝΩΘ§–Έ≥…1 mol H-ClΦϋΖ≈≥ω431 kJΡήΝΩΓΘ‘ρH2”κCl2Ζ¥”Π≤ζ…ζHClΒΡΖ¥”Π»»ΓςH=436 kJ +243 kJ -2ΓΝ431 kJ=-183 kJΘ§Ι ΗΟΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣΘΚH2(g)ΘΪCl2(g)=2HCl(g) ΠΛH=Θ≠183 kJ/molΘΜ
ΔΎ”…”ΎΖ¥”ΠΈοΒΡΉήΡήΝΩ±»…ζ≥…ΈοΒΡΉήΡήΝΩΗΏΘ§‘ρΗΟΖ¥”ΠΖΔ…ζ ±Ζ≈≥ω»»ΝΩΘ§Ζ¥”ΠΈΣΖ≈»»Ζ¥”ΠΘ§ΥΒΟςΖ¥”ΠΈοΒΡΉήΡήΝΩ±»…ζ≥…ΈοΒΡΉήΡήΝΩΗΏΘ§Φ¥Ζ¥”ΠΈοΒΡΉήΡήΝΩΘΨ…ζ≥…ΈοΒΡΉήΡήΝΩΘΜ
(3)ΗυΨίΆΦ ΨΩ…÷ΣCH4»Φ…’≤ζ…ζΤχΧ§Υ°ΒΡ»»Μ·―ßΖΫ≥Χ ΫΔΌΈΣΘΚ CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΠΛH=Θ≠802 kJ/molΘΜS’τΤχΆξ»Ϊ»Φ…’≤ζ…ζSO2ΤχΧεΒΡ»»Μ·―ßΖΫ≥Χ ΫΔΎΈΣΘΚS(g)+O2(g)=SO2(g) ΠΛH=Θ≠577 kJ/molΘ§ΗυΨίΗ«ΥΙΕ®¬…Θ§ΫΪΔΌ-2ΓΝΔΎΘ§’ϊάμΩ…ΒΟΘΚCH4Ω…“‘ΜΙ‘≠SO2…ζ≥…ΒΞ÷ S(g)ΓΔH2O(g)ΚΆCO2ΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣΘΚCH4(g)+2SO2(g)=2S(g)+CO2(g)+2H2O(g) H=+352 kJ/molΘΜ
(4)ΗυΨί…œ ωΆΤΕœΩ…÷ΣΘΚAΈΣSiΘ§BΈΣSiO2Θ§CΈΣH2SiO3Θ§DΈΣNa2SiO3Θ§E «CaSiO3ΓΘ
ΔΌAΈΣSiΘ§BΈΣSiO2Θ§SiO2”κΫΙΧΩ‘ΎΗΏΈ¬œ¬Ζ¥”Π≤ζ…ζSiΚΆCOΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣΘΚSiO2ΘΪ2C![]() SiΘΪ2COΓϋΘΜ
SiΘΪ2COΓϋΘΜ
BΈΣSiO2Θ§E «CaSiO3Θ§SiO2”κCaCO3‘ΎΗΏΈ¬œ¬Ζ¥”Π≤ζ…ζCaSiO3ΚΆCO2Θ§Ζ¥”ΠΖΫ≥Χ ΫΈΣΘΚCaCO3ΘΪSiO2![]() CaSiO3ΘΪ
CaSiO3ΘΪ
ΔΎCΈΣH2SiO3Θ§DΈΣNa2SiO3Θ§”…”ΎΧΦΥαΒΡΥα–‘±»ΙηΥα«ΩΘ§œρΙηΥαΡΤ»ή“Κ÷–Ά®»κCO2ΤχΧεΘ§»τΆ®»κ…ΌΝΩCO2ΤχΧεΘ§Ζ¥”Π≤ζ…ζNa2CO3ΚΆH2SiO3Θ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΘΚSiO32-ΘΪH2OΘΪCO2=H2SiO3ΓΐΘΪCO32-ΘΜ»τΆ®»κΙΐΝΩCO2ΤχΧεΘ§ΖΔ…ζΗ¥Ζ÷ΫβΖ¥”Π≤ζ…ζNaHCO3ΚΆH2SiO3Θ§ΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΘΚSiO32-ΘΪ2H2OΘΪ2CO2=H2SiO3ΓΐΘΪ2HCO3-ΘΜ
(5)ΗυΨίΙηΥα―Έ”Ο―θΜ·Έο–Έ Ϋ±μ Ψ ±ΒΡΙφ¬…Θ§Mg6Si4O10(OH)8”Ο―θΜ·ΈοΒΡ–Έ ΫΩ…±μ ΨΈΣ6MgO4SiO24H2OΓΘ

 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ –Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
–Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗΓΨΧβΡΩΓΩ“ΜΕ®Έ¬Ε» ±Θ§œρ»ίΜΐΈΣ2LΒΡΟή±’»ίΤς÷–≥δ»κ“ΜΕ®ΝΩΒΡSO2ΚΆO2Θ§ΖΔ…ζΖ¥”Π2SO2(gΘ©+O2(gΘ©![]() 2SO3(gΘ© HΘΫΘ≠196kJΓΛmoL1Θ§“ΜΕΈ ±ΦδΚσ¥οΤΫΚβΘ§Ζ¥”ΠΙΐ≥Χ÷–≤βΕ®ΒΡ≤ΩΖ÷ ΐΨίΦϊœ¬±μΘΚ
2SO3(gΘ© HΘΫΘ≠196kJΓΛmoL1Θ§“ΜΕΈ ±ΦδΚσ¥οΤΫΚβΘ§Ζ¥”ΠΙΐ≥Χ÷–≤βΕ®ΒΡ≤ΩΖ÷ ΐΨίΦϊœ¬±μΘΚ
Ζ¥”Π ±Φδ/min | n(SO2Θ©/mol | n(O2Θ©/mol |
0 | 2 | 1 |
5 | 1.2 | |
10 | 0.4 | |
15 | 0.8 |
œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A. Ζ¥”Π‘Ύ«Α5minΒΡΤΫΨυΥΌ¬ ΈΣv (SO2Θ©=0.08molΓΛL1ΓΛmin1
B. ±Θ≥÷Έ¬Ε»≤Μ±δΘ§œρΤΫΚβΚσΒΡ»ίΤς÷–‘Ό≥δ»κ1molSO2ΚΆ0.5molO2 ±Θ§v (’ΐΘ©ΘΨ v (ΡφΘ©
C. ΗΟΈ¬Ε»Θ§Ζ¥”ΠΒΡΤΫΚβ≥Θ ΐΈΣ11.25LΓΛmolΘ≠1
D. œύΆ§Έ¬Ε»œ¬Θ§Τπ Φ ±œρ»ίΤς÷–≥δ»κ1.5mol SO3Θ§¥οΤΫΚβ ±SO3ΒΡΉΣΜ·¬ ΈΣ40%