题目内容
【题目】2019年3月21日是第二十七届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关图像如下所示:
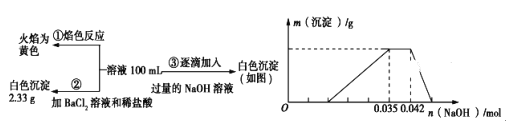
请回答下列问题:
(1)焰色反应是_________ (填“物理”或“化学”)变化;实验②中产白色沉淀是_________ (填化学式)。
(2)原溶液中一定存在的离子有________________,可能存在的离子有________________,一定不存在的离子有________________ (写化学式)。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为________________
(4)若通过实验确定原废水中c(Na+)=0.14 mol·L1,试判断原废水中NO3是否存在?________________(填“存在”“不存在”或“不确定”)。 若存在,c(NO3)=___________mol·L1。(若不存在或不确定则此空不填)
【答案】物理 BaSO4 Na+、SO42-、H+、Al3+、NH4+ NO3- Fe3+、Mg2+、CO32- 1:1 存在 0.36
【解析】
根据溶液颜色及焰色反应等实验现象分析溶液中离子存在情况;根据图像中沉淀的变化及消耗的氢氧化钠的物质的量分析计算溶液中存在的离子及其物质的量;根据溶液的电中性分析判断溶液中可能存在的离子,并计算其物质的量。
(1)焰色反应是物理变化;实验②中加入BaCl2和盐酸,产白色沉淀是不溶液盐酸的BaSO4,故答案为:物理;BaSO4;
(2)Fe3+呈黄色,则肯定不存在,实验①中焰色反应为黄色,则确定存在Na+;实验②中加入BaCl2和盐酸,产白色沉淀是不溶液盐酸的BaSO4,确定存在SO42-,根据实验③中沉淀的变化,可以分析知发生的反应依次为:H++OH-=H2O、Al3++3OH-=Al(OH)3↓、NH4++OH-=NH4H2O、Al(OH)3+OH-=AlO2-+2H2O则确定有H+、Al3+、NH4+,沉淀完全溶解,则没有Mg2+,因为CO32-与Al3+不能共存,所以无CO32-;所以原溶液中一定存在的离子有Na+、SO42-、H+、Al3+、NH4+;一定不存在的离子有Fe3+、Mg2+、CO32-;可能存在的离子是NO3-,故答案为:Na+、SO42-、H+、Al3+、NH4+;NO3-;Fe3+、Mg2+、CO32-;
(3)根据图像中沉淀不变的部分及NH4++OH-=NH4H2O分析知:n(NH4+)=n(OH-)=0.042mol-0.035mol=0.007mol;根据图像中生成沉淀部分及Al3++3OH-=Al(OH)3↓分析知:c(Al3+)=1/3n(OH-)=1/3×(0.042mol-0.035mol)×3=0.007mol,则原溶液中c(NH4+)与c(Al3+)的比值等于物质的量之比:0.007mol:0.007mol=1:1,故答案为:1:1;
(4)根据硫酸钡沉淀2.33g,n(SO42-)=![]() ,根据电荷守恒,阴离子电荷总物质的量为0.01mol×2=0.02mol,阳离子电荷总物质的量为n(H+)+n(Al3+)+n(NH4+)+n(Na+)=0.014mol+0.007×3mol+0.007mol+0.14mol/L×0.1L=0.056mol,则原废水中存在NO3-,c(NO3-)=
,根据电荷守恒,阴离子电荷总物质的量为0.01mol×2=0.02mol,阳离子电荷总物质的量为n(H+)+n(Al3+)+n(NH4+)+n(Na+)=0.014mol+0.007×3mol+0.007mol+0.14mol/L×0.1L=0.056mol,则原废水中存在NO3-,c(NO3-)=![]() =0.36mol/L;故答案为:存在;0.36。
=0.36mol/L;故答案为:存在;0.36。

【题目】合成氨原料可以由天然气制取。其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1 m3(标准状况)CH4按上式完全反应,产生H2_________mol。(精确到0.1)
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V m3(标准状况)的取值范围为________。
(3)CH4和H2O(g)及富氧空气(O2含量较高的空气)混合反应,产物气体组成如下表:
气体 | CO | H2 | N2 | O2 |
体积(L) | 25 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比,V(O2):V(N2)=________。
(4)若CH4和H2O(g)及(3)题中的富氧空气混合反应,产物气体中V(H2):V(N2)=3:1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为_______。