题目内容
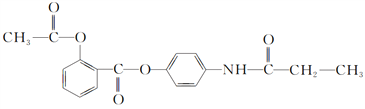
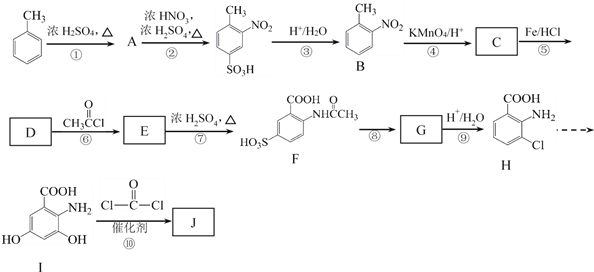
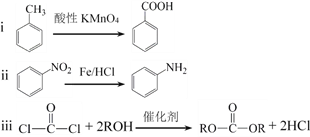
【题目】《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯![]() 是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
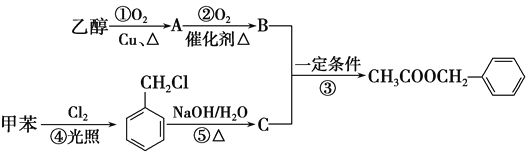
(1)B、C的结构简式分别为______________、________________。
(2)写出反应①、④的化学方程式:
①_____________________;④______________________。
(3)反应③、⑤的反应类型分别为③________,⑤____________。
(4)反应________(填序号)原子的理论利用率为100%,符合“绿色化学”的要求。
(5)乙酸苯甲酯的同分异构体中能与碳酸氢钠反应生成气体的有________种。
【答案】 CH3COOH ![]() 2CH3CH2OH+O2
2CH3CH2OH+O2![]() 2CH3CHO+2H2O 略 酯化(或取代)反应 水解(或取代)反应 ② 14
2CH3CHO+2H2O 略 酯化(或取代)反应 水解(或取代)反应 ② 14
【解析】由合成流程可以知道,乙醇在Cu或Ag催化作用下加热反应生成![]() ,
,![]() 继续被氧化为
继续被氧化为![]() ,甲苯光照下发生取代反应生成
,甲苯光照下发生取代反应生成![]() ,
,![]() 在碱性条件下水解生成C为
在碱性条件下水解生成C为![]() ,在一定条件下与
,在一定条件下与![]() 发生酯化反应生成
发生酯化反应生成![]() ,
,
(1)由以上分析可以知道B为![]() ,C为
,C为![]() ,因此,本题正确答案是:
,因此,本题正确答案是:![]() ;
;![]() ;
;
(2)反应①为乙醇催化氧化,生成乙醛和水,反应为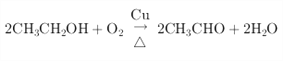 ,
,
反应④的方程式为![]()
![]()
![]()
![]() ,
,
因此,本题正确答案是: ;
; ![]()
![]()
![]()
![]() ;
;
(3)反应③的化学方程式![]() ,为酯化反应或取代反应,⑤为氯代烃的水解反应,也为取代反应,
,为酯化反应或取代反应,⑤为氯代烃的水解反应,也为取代反应,
因此,本题正确答案是:酯化(或取代)反应;水解(或取代)反应。
(4)由 知反应②是乙醛的催化氧化反应,原子的理论利用率能达100%,符合“绿色化学”的要求,所以答案: ②。
知反应②是乙醛的催化氧化反应,原子的理论利用率能达100%,符合“绿色化学”的要求,所以答案: ②。
(5) 能与碳酸氢钠反应生成气体一定含有羧基,其乙酸苯甲酯的同分异构体有
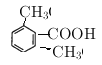 (6种)
(6种)![]() (3种)
(3种)![]() (2种)
(2种)
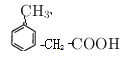 (3种)答案:14种。
(3种)答案:14种。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)===HCHO(g)+H2(g) ΔH=+84 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1
①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:______________________________________________。
②在上述制备甲醛时,常向反应器中通入适当过量的氧气,其目的_________________。
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)==CH3OH(g),已知某些化学键的键能数据如下表:
化学键 | C—C | C—H | H—H | C—O | C≡O | O—H |
键能/(kJ·mol-1) | 348 | 413 | 436 | 358 | x | 463 |
请回答下列问题:
①图1中曲线a到曲线b的措施是_________。
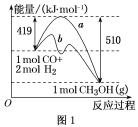
②已知CO中的C与O之间为叁键,其键能为x kJ/mol,则x=________。
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为______________________________________。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为________。
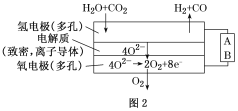
(4)电解水蒸气和CO2产生合成气(H2