题目内容
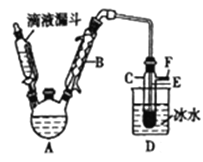
【题目】下图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置。有关数据见下表。
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/g.cm-3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)制备操作中,加入的浓硫酸必须进行稀释,其目的是_____(填字母)。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(2)己知加热温度较低时NaBr与硫酸反应生成NaHSO4,写出加热时A中发生的主要反应的化学方程式:________________。
(3)仪器B的名称是________,冷却水应从B的____(填“上“或“下")口流进。
(4)反应生成的溴乙烷应在______(填“A"或"C")中。
(5)若用浓的硫酸进行实验时,得到的溴乙烷呈棕黄色,最好选择下列_____(填字母)溶液来洗涤产品。
a氢氧化钠 b.碘化亚铁 c.亚硫酸钠 d.碳酸氢钠
洗涤产品时所需要的玻璃仪器有_______________。
【答案】 abc CH3CH2OH+NaBr+H2SO4![]() NaHSO4+CH3CH2Br+H2O 球形冷凝管 下 C c 分液漏斗、烧杯
NaHSO4+CH3CH2Br+H2O 球形冷凝管 下 C c 分液漏斗、烧杯
【解析】(1)在浓硫酸、加热条件下,乙醇可以发生消去反应生成乙烯,也可以发生分子间脱水生成醚,浓硫酸具有强氧化性可以氧化得到溴单质,反应会有水生成,反应中会放出大量的热,容易使HBr挥发等,故制备操作中,加入的浓硫酸必需进行稀释,其目的是:减少副产物烯和醚的生成,减少Br2的生成,减少HBr的挥发,故选:abc;
(2)加热温度较低时NaBr与硫酸反应生成NaHSO4与HBr,HBr与乙醇发生取代反应生成CH3CH2Br与水,反应反应方程式为:CH3CH2OH+NaBr+H2SO4![]() NaHSO4+CH3CH2Br+H2O,故答案为:CH3CH2OH+NaBr+H2SO4
NaHSO4+CH3CH2Br+H2O,故答案为:CH3CH2OH+NaBr+H2SO4![]() NaHSO4+CH3CH2Br+H2O;
NaHSO4+CH3CH2Br+H2O;
(3)由仪器结构特征,可知仪器B为球形冷凝管,应采取逆流原理通入冷凝水,进行充分冷凝回流,即冷却水应冷凝管的下口流入,从上口流出,故答案为:球形冷凝管;下;
(4)反应得到溴乙烷沸点很低,在C中用冰水冷却收集,故答案为:C;
(5)用浓的硫酸进行实验时,得到的溴乙烷呈棕黄色,是因为溶解了溴,洗涤除去溴:a.氢氧化钠可以与溴反应,但也会引起溴乙烷水解,故a错误;b.溴与碘化亚铁会生成碘单质,溴乙烷会溶解碘单质,故b错误;c.加亚硫酸钠只与溴发生反应,不与溴乙烷反应,故c正确;d.碳酸氢钠溶液呈碱性,会和溴单质、溴乙烷反应,故d错误;洗涤后需要通过分液进行分离,洗涤需要在分液漏斗中进行,用烧杯接取水层溶液,故答案为:c;分液漏斗、烧杯。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案


