题目内容
【题目】国家航天局计划2020年实施火星探测任务。据了解火星上存在大量的含氮化合物科学家推测火星生命可能主要以氮、碳、硅、铜为基体构成。
(1)邻氨基吡啶(![]() )的铜配合物在有机不对称合成中起催化诱导效应。
)的铜配合物在有机不对称合成中起催化诱导效应。
①邻氨基吡啶中所有元素的电负性由小到大的顺序为__(填元素符号)。设NA为阿伏加德罗常数的值,1mol![]() 中含有σ键的数目为__。
中含有σ键的数目为__。
②一定条件下-NH2可以被氧化成-NO2,-NH2中N原子的杂化方式为__杂化。
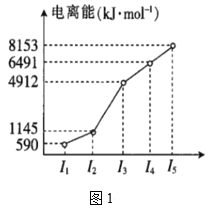
(2)第四周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素的基态原子电子排布式为___。
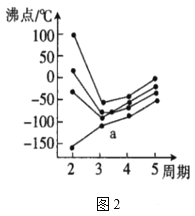
①嘌呤中轨道之间的夹角∠1比∠2大,原因是___。
②![]() 分子中的大π键可以用符号
分子中的大π键可以用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为__。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为__。
(3)火星岩石中存在大量的氮化镓,氮化镓为六方晶胞,结构如图3所示。
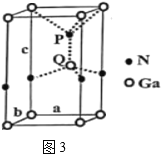
若该晶体密度为dg·cm-3,晶胞参数a=b≠c(单位:nm),a、b夹角为120o,阿伏加德罗常数的值为NA,则晶胞参数c=__(写出代数式)nm。
【答案】H<C<N 13NA sp2 1s22s22p63s23p64s2 孤电子对与成键电子对之间的斥力大于成键电子对之间的斥力 ![]()
![]()
【解析】
(1) ①邻氨基吡啶中含有的元素为H、C、N,非金属性H<C<N,电负性与非金属性成正比。![]() 分子中含有σ键的数目等于原子间形成的键数(两个原子间只能形成1个σ键)。
分子中含有σ键的数目等于原子间形成的键数(两个原子间只能形成1个σ键)。
②-NH2中N原子的杂化轨道数为N原子的价层电子对数。
(2)从图中可以看出,该原子容易失去2个电子,从第3个电子起很难失去。
①嘌呤中轨道之间的夹角∠1比∠2大,夹角小,说明排斥作用大。
②![]() 分子中的大π键由5个原子6个电子形成。
分子中的大π键由5个原子6个电子形成。
(3) 在1个氮化镓晶胞中,含有2个“GaN”,晶胞的体积为![]() nm3,晶胞的体积也可表示为
nm3,晶胞的体积也可表示为![]() ,利用两式,可求出c。
,利用两式,可求出c。
(1) ①邻氨基吡啶中含有的元素为H、C、N,非金属性H<C<N,则电负性由小到大的顺序为H<C<N。1个![]() 分子中含有13个σ键,则1mol
分子中含有13个σ键,则1mol![]() 中含有σ键的数目为13NA。答案为:H<C<N;13NA;
中含有σ键的数目为13NA。答案为:H<C<N;13NA;
②-NH2中N原子形成2个共价键,还有1对孤对电子,N原子的价层电子对数为3,则N原子的杂化方式为sp2杂化。答案为:sp2;
(2)从图中可以看出,该原子容易失去2个电子,从第3个电子起很难失去,所以第3个电子不在4p轨道上,只能在3p轨道,从而得出该元素的基态原子电子排布式为1s22s22p63s23p64s2。答案为:1s22s22p63s23p64s2;
①嘌呤中轨道之间的夹角∠1比∠2大,夹角小,说明排斥作用大,则原因是孤电子对与成键电子对之间的斥力大于成键电子对之间的斥力。答案为:孤电子对与成键电子对之间的斥力大于成键电子对之间的斥力;
②![]() 分子中的大π键由5个原子6个电子形成,则该吡啶中的大π键可表示为
分子中的大π键由5个原子6个电子形成,则该吡啶中的大π键可表示为![]() 。答案为:
。答案为:![]() ;
;
(3) 在1个氮化镓晶胞中,含有2个“GaN”,晶胞的体积为![]() nm3,晶胞的体积也可表示为
nm3,晶胞的体积也可表示为![]() ,由此得出
,由此得出![]() nm3=
nm3=![]() ,从而求出c=
,从而求出c=![]() 。答案为:
。答案为:![]() 。
。

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案