题目内容
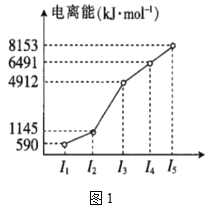
【题目】常温下,向20mL 0.1mol·L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的c(H+)随加入硫酸的体积变化如图所示。下列说法不正确的是
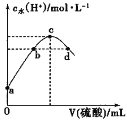
A.若a点对应水电离的c(H+)=1.0×10-11mol·L-1,则此时氨水的电离程度为1%
B.c点时氨水与硫酸恰好完全反应
C.c点对应溶液中:c(H+)-c(OH-)=c(NH3·H2O)
D.若b、d点对应水电离的c(H+)=1.0×10-7mol·L-1,则两溶液中均存在:c(NH4+)=2c(SO42-)
【答案】D
【解析】
A.水电离的氢离子浓度为1.0×10-11 molL-1,由Kw可知溶液中的氢氧根离子的浓度为1.0×10-3 molL-1,则氨水的电离度为![]() ×100%=1%,故A正确;
×100%=1%,故A正确;
B.c点水的电离程度最大,说明恰好生成硫酸铵,即c点时氨水与硫酸恰好完全反应,故B正确;
C.c点溶液中溶质为硫酸铵,溶液中质子守恒为c(H+)═c(NH3H2O)+c(OH-),则c(H+)-c(OH-)═c(NH3H2O),故C正确;
D.c点硫酸与氨水恰好反应,则b点硫酸不足,d点硫酸过量,溶液中氢离子浓度大于1.0×10-7 molL-1,d点时:c(NH4+)≠2c(SO42-),故D错误。
故选:D。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g),下列说法正确的是
CH3OH(g),下列说法正确的是
容器 | 温度/K | 物质的平衡浓度/mol/L | |||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
I | 400 | 0.20 | 0.10 | 0 | 0.080 |
II | 400 | 0.40 | 0.20 | 0 | |
III | 500 | 0 | 0 | 0.10 | 0.025 |
A.该反应的正反应吸热
B.达到平衡时,容器I中反应物转化率比容器II中的大
C.达到平衡时,容器II中c(H2)大于容器I中c(H2)的两倍
D.达到平衡时,容器III中的反应速率比容器I中的大