��Ŀ����
����Ŀ����ɫ����N2O4��һ��ǿ��������Ϊ��Ҫ�Ļ���ƽ���֮һ��N2O4��NO2ת�����Ȼ�ѧ����ʽΪN2O4��g��![]() 2NO2��g�� ��H����24.4 kJ/ mol��
2NO2��g�� ��H����24.4 kJ/ mol��
��1����һ����N2O4Ͷ��̶��ݻ�����������У�����������˵����Ӧ�ﵽƽ�����____
a v����N2O4����2v����NO2�� b ��ϵ��ɫ����
c ����ƽ����Է����������� d �����ܶȲ���
��2��ƽ�ⳣ��K���÷�Ӧ��ϵ���������ʷ�ѹ��ʾ����K����ʽ����ƽ���ѹ����ƽ��Ũ�ȣ���ѹ����ѹ�����ʵ�������[���磺p��NO2����p����x��NO2��]��д��������Ӧƽ�ⳣ��Kp����ʽ_________����p�������������ʵ���������x��ʾ����
��3��������Ӧ�У�����Ӧ����v����k����p��N2O4�����淴Ӧ����v����k����p2��NO2��������k����k��Ϊ���ʳ�������KpΪ_______����k����k����ʾ��������һ����N2O4Ͷ����������к��º�ѹ�ֽ⣨�¶�298K��ѹǿ100kPa������֪��������k����4.8��104s��1����N2O4�ֽ�10%ʱ��v����_______kPa��s��1�������������λ��Ч���֣�
��4������ܱ������з���һ����N2O4��ά����ѹǿp0�㶨�����¶�ΪTʱ��ƽ��ʱN2O4�ֽ�ٷ���Ϊ���������¶Ȳ��䣬���ܱ������г������N2O4��ά����ѹǿ��2p0�����·ֽ⣬��N2O4��ƽ��ֽ��ʵı���ʽΪ________��
���𰸡�bc ![]()
![]() 3.9��106
3.9��106 ![]()
��������
��a. N2O4������NO2������������ͬ�������ʱȲ����ڼ���ϵ���ȣ�b. ��ϵ��ɫ��ʼҪ�䣬�������䣻c. ����ƽ����Է����������������������ʵ������������䣬���ʵ������ӣ�����ƽ����Է����������٣�d. �����ܶȵ���������������������������䣬����������䣬�ܶ�ʼ�ղ��䡣
�Ƹ��ݷ�Ӧ�õ�ƽ�ⳣ����
�Ǹ���v�� =v�����ó�Kp���ٸ�����֪�� N2O4�� NO2���ʵ������м�������Ӧ���ʡ�
���¶���ͬ��ǰ�����ν��������ǰ�����ε�ƽ�ⳣ����ͬ������ϵ���㡣
��a. N2O4������NO2������������ͬ�������ʱȲ����ڼ���ϵ���ȣ�����˵���ﵽƽ�⣬��a���������⣻b. ��ϵ��ɫ��ʼҪ�䣬�������䣬��˵���ﵽƽ�⣬��b�������⣻c. ����ƽ����Է����������������������ʵ������������䣬���ʵ������ӣ�����ƽ����Է����������٣��������䣬��ﵽƽ�⣬��c�������⣻d. �����ܶȵ���������������������������䣬����������䣬�ܶ�ʼ�ղ��䣬����˵���ﵽƽ�⣬��d���������⣻������������Ϊ��bc��
��������Ӧƽ�ⳣ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��������Ӧ�У�����Ӧ����v����k����p��N2O4�����淴Ӧ����v����k����p2��NO2��������k����k��Ϊ���ʳ�����v�� =v������Kp=![]() ������һ����N2O4Ͷ����������к��º�ѹ�ֽ⣨�¶�298K��ѹǿ100kPa������֪��������k����4.8��104s��1����N2O4�ֽ�10%ʱ�����迪ʼ��1mol N2O4�ֽ�0.1mol������0.2mol NO2��
������һ����N2O4Ͷ����������к��º�ѹ�ֽ⣨�¶�298K��ѹǿ100kPa������֪��������k����4.8��104s��1����N2O4�ֽ�10%ʱ�����迪ʼ��1mol N2O4�ֽ�0.1mol������0.2mol NO2��![]() ���ʴ�Ϊ��3.9��106��
���ʴ�Ϊ��3.9��106��
���¶���ͬ�����ǰ�����ε�ƽ�ⳣ����ͬ�������¶Ȳ��䣬���ܱ������г������N2O4��ά����ѹǿ��2p0�����·ֽ⣬��N2O4��ƽ��ֽ���Ϊy��

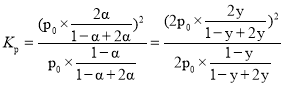 �����
�����![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��

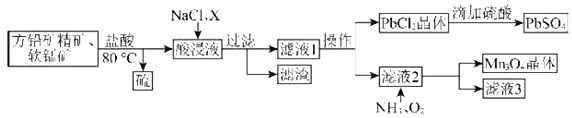
����Ŀ����������(NaNO2)��ۿ���ʳ��������ζ����һ�ֳ��õķ�ɫ���ͷ�������ʹ�ù�����ʹ���ж��������϶�ʳƷ���������Ƶ����������ںܵ͵�ˮƽ�ϡ�ijѧϰС����������������������ʵ�飺
��ʵ����Ʊ�NaNO2
��С���������֪��2NO��Na2O2=2NaNO2��2NO2��Na2O2=2NaNO3��
�Ʊ�װ����ͼ��ʾ(�г�װ����ȥ)��
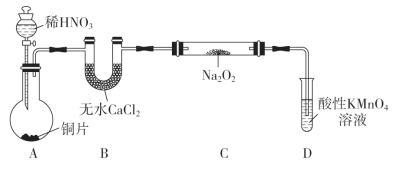
(1)װ��D�ɽ�ʣ���NO������NO3����������Ӧ�����ӷ���ʽΪ____________��
(2)���û��Bװ�ã�C�з����ĸ���Ӧ��_____________��____________��
(3)��ͬѧ�����װ�����������ú����ʵ�飬�����Ƶõ�NaNO2�л��н϶��NaNO3���ʡ����ǽ������ʵ��ĸĽ����Ľ��������NaNO2�Ĵ��ȣ�����Ľ���ʩ��________________________________��
��ʵ�������ⶨ��ȡ����Ʒ��NaNO2�ĺ���
���裺
a����5���б�ŵĴ��̶��Թ�(��ɫ��)�зֱ���벻ͬ����NaNO2��Һ��������1 mL��M��Һ(M��NaNO2���Ϻ�ɫ��NaNO2Ũ��Խ����ɫԽ��)���ټ�����ˮ���������Ϊ10 mL�����Ƴɱ�ɫ�ף�
�Թܱ�� | �� | �� | �� | �� | �� |
NaNO2����/(mg��L��1) | 0 | 20 | 40 | 60 | 80 |
b������0.10 g�Ƶõ���Ʒ������ˮ���500 mL��Һ��ȡ5 mL����Һ������1 mL M��Һ���ټ�����ˮ��10 mL�������ɫ�ױȽϡ�
(4)����b�бȽϽ���ǣ�����Һ��ɫ��۱�ɫ����ͬ�����ͬѧ�Ƶõ���Ʒ��NaNO2������������________��
(5)��Ŀ�ӱ�ɫ��֤��ά����C������Ч����NaNO2�ĺ�������Ʋ��������ʵ�鱨�档
ʵ�鷽�� | ʵ������ | ʵ����� |
ȡ5 mL����Һ������______________�����ټ���1 mL M��Һ��_______________��������۱�ɫ�Ա� | _______________ | ά����C������Ч����NaNO2�ĺ��� |