��Ŀ����
����Ŀ���±���Ԫ�����ڱ���һ����,����������10��Ԫ��,������¸�С�⡣
������ ���ڡ��� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
1 | H | |||||||
2 | C | N | F | Ne | ||||
3 | Na | Mg | Al | S | Cl |
(1)��������ǿ��Ԫ����______(��Ԫ�ط���)��
(2)�����Ԫ�ص�ԭ�ӽṹʾ��ͼΪ________��
(3)��3����Ԫ���У�������������Ӧ��ˮ����������Ե�Ԫ����______(��Ԫ������)��
(4)Na��Mg����Ԫ���У�ԭ�Ӱ뾶�ϴ����______��
(5)��3�����У�ijԪ�ص�һ�����������γ��������Ҫ���ʣ���������Ļ�ѧʽΪ_______��
(6)��ҵ�Ͽ�����Cl2��H2����ȡ����÷�Ӧ�ķ���ʽΪ_______________________________��
(7)HF��HCl���ȶ��Խ�ǿ����_________��
(8)��̼����Ԫ���γɵ�����л���Ļ�ѧʽΪ_____����������̼Ԫ������Ԫ�ص�������Ϊ_________������ӿռ乹��Ϊ_____________��
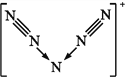
(9)����![]() �ͳ�����
�ͳ�����![]() ���ֺ��ض������������ⵯ��ԭ�ϣ���������������֮��Ϊ____��
���ֺ��ض������������ⵯ��ԭ�ϣ���������������֮��Ϊ____��
���𰸡�Na 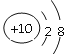 �� Na SO2 H2+Cl2
�� Na SO2 H2+Cl2![]() 2HCl HF CH4 3��1 �������� 1��2
2HCl HF CH4 3��1 �������� 1��2
��������
��1��ͬ����������ҽ����Լ������ǽ�������ǿ��ͬ�������϶��½�������ǿ���ǽ����Լ�����ϡ�����廯ѧ��������ã�
��2������Ԫ�ش����ȶ��ṹ����ѧ��������ã�
��3���������ᷴӦ�����κ�ˮ��Ҳ����ǿ�Ӧ�����κ�ˮ����������Ϊ���ԣ�
��4��ͬһ���ڴ�����ԭ�Ӱ뾶��С��
��5���γ��������Ҫ�����Ƕ�������
��6�����������������Ȼ��⣻
��7��ͬһ����Ԫ�ش��ϵ��·ǽ����Լ������ǽ�����Խǿ����̬�⻯��Խ�ȶ���
��8����̼����Ԫ���γɵ�����л���ΪCH4���ݴ˷�����
��9������������=������-���������㣻
��1��ͬ����������ҽ����Լ������ǽ�������ǿ��ͬ�������϶��½�������ǿ���ǽ����Լ�����ϡ�����廯ѧ��������ã���˱����н�������ǿ��Ԫ����Na��
�𰸣�Na
��2��NeΪ����Ԫ�أ�����������Ϊ8�������ȶ��ṹ����ѧ���������Ԫ�أ�ԭ�ӽṹʾ��ͼΪ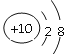 ��
��
�𰸣�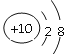
��3�����������������ᷴӦ�����κ�ˮ��Ҳ����ǿ�Ӧ�����κ�ˮ���ʾ������Ե�Ԫ����Al��
�𰸣�����
��4��ͬһ���ڴ�����ԭ�Ӱ뾶��С����Na��ԭ�Ӱ뾶����Mgԭ�Ӱ뾶��
�𰸣�Na��
��5���γ��������Ҫ�����Ƕ�������ѧʽΪSO2��
�𰸣�SO2
��6��Cl2��H2����ȡ���ᣬ�÷�Ӧ�ķ���ʽΪH2+Cl2![]() 2HCl��
2HCl��
�𰸣�H2+Cl2![]() 2HCl��
2HCl��
��7��ͬһ����Ԫ�ش��ϵ��·ǽ����Լ������ǽ�����Խǿ����̬�⻯��Խ�ȶ���
�𰸣�HF��
��8����̼����Ԫ���γɵ�����л���Ļ�ѧʽΪCH4����������̼Ԫ������Ԫ�ص�������Ϊ12:4=3:1������ӿռ乹��Ϊ�������壻
�𰸣�CH4 �� 3:1 �� �������壻
��9��)����![]() ������Ϊ2-1=1��������
������Ϊ2-1=1��������![]() ������Ϊ3-1=2��������֮��1:2��
������Ϊ3-1=2��������֮��1:2��
�𰸣�1:2��

 ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д� â���̸����������������ϵ�д�
â���̸����������������ϵ�д�����Ŀ����̼���ʵļ�ֵ��ת��������������̼���Ϳɳ����Է�չ��������Ҫ���о���ֵ����ش��������⣺
(1)��֪CO�����л�ѧ��ΪC��O����صĻ�ѧ�������������£�
��ѧ�� | H��O | C��O | C=O | H��H |
E/(kJ��mol1) | 463 | 1075 | 803 | 436 |
CO(g)+H2O(g)CO2(g)+H2(g) ��H=__kJ��mol1��
�������������COƽ��ת���ʵĴ�ʩ��__(����)��
a.����ѹǿ b.�����¶� c.���ԭ������H2O�ı��� d.ʹ�ø�Ч����
(2)�ö��Ե缫���KOH��Һ���ɽ������е�CO2ת��Ϊ�����(HCOO)��Ȼ���һ�������Ƶ���Ҫ�л�����ԭ�ϼ��ᡣCO2������Ӧ�ĵ缫��ӦʽΪ__������������ת��1mol���ӣ�����������������(��״��)Ϊ__L��
(3)�ұ���������ȡ����ϩ�ķ�ӦΪ��
![]() (g)+CO2(g)
(g)+CO2(g)![]() (g)+CO(g)+H2O(g)���䷴Ӧ�������£�
(g)+CO(g)+H2O(g)���䷴Ӧ�������£�

��һ���¶��£�������ܱ������г���2mol�ұ���2molCO2����ʼѹǿΪp0��ƽ��ʱ���������������ʵ���Ϊ5mol���ұ���ת����Ϊ__����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=__��[�����ѹ(p��)=������ѹ(p��)�������������]
���ұ�ƽ��ת������p(CO2)�Ĺ�ϵ��ͼ��ʾ��������ұ�ƽ��ת��������p(CO2)�仯���仯��ԭ��__��