题目内容
【题目】已知:A.金刚石、B.MgF2、C.NH4Cl、D.NaNO3、E.干冰、F.固体碘,填写下列空白。(用序号填写)
(1)熔化时不需破坏化学键的是________,熔化时只需破坏共价键的是________,熔点最低的是________,
晶体中既存在离子键又存在共价键的是________。
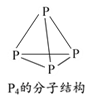
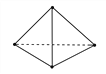
(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 mol N—N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量。根据以上信息和数据,则1 mol N4生成N2的ΔH=______ kJ·mol-1
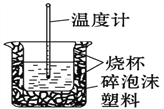
(3) 50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的NaOH溶液在如图所示的装置中进行中和反应。
请回答下列问题:
从实验装置上看,图中尚缺少的一种玻璃仪器是_____,烧杯间填满碎泡沫塑料的作用是______。大烧杯上如不盖硬纸板,则求得的中和热数值_______(填“偏大”、“偏小”或“无影响”)。
【答案】 EF A E CD -882 环形玻璃搅拌棒 保温隔热,防止热量散失 偏小
【解析】一般来说,活泼金属元素与非金属元素形成离子键,非金属元素之间形成共价键,(1)分子晶体熔化不破坏化学键,即EF中熔化不破坏化学键,原子晶体熔化破坏共价键,则A熔化破坏共价键,一般来说,原子晶体熔点最高,分子晶体熔点较低,E的相对分子质量小于F,则E的熔点最低;离子晶体中一定存在离子键,C、D中非金属元素之间形成共价键;(2)由题意知,N≡N的键能为942kJ/mol,N-N键的键能为167kJ/mol,则1 mol N4生成N2的反应为: N4(g)=2N2(g),反应热等于反应物的总键能减去生成物的总键能,故反应热△H=6×167kJ/mo l -2×942kJ/mol =-882kJ/mol;(3)根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器;烧杯间填满碎泡沫塑料的作用是保温隔热,防止热量散失;大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小。

【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 | 实验装置 |
A | 稀硫酸 | Na2S | AgNO3与AgCl的溶液 | Ksp(AgCl)>Ksp(Ag2S) |
|
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D