题目内容
【题目】根据下图所示实验回答下列问题:
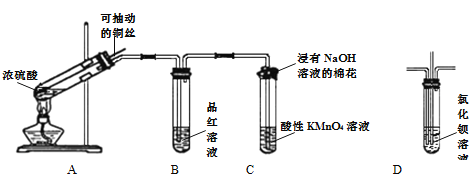
(1)装置A中试管内发生反应的化学方程式是_________________________________。
(2)根据装置B中的现象可以证明SO2具有__________性,反应一段时间后,将装置B中试管加热,可以观察到_______________________。
(3)装置C中试管口的棉花团上发生反应的离子方程式为________________________。
(4)如果将装置B换成装置D,并从直立导管中向氯化钡溶液中通入另一种气体,产生白色沉淀,则这种气体可能是_________________(填一种即可)。
【答案】Cu+2H2SO4(浓) ![]() CuSO4+2H2O+ SO2↑ 漂白 溶液由无色变成红色 SO2+2OH-=SO32-+H2O NO2(或Cl2、或O2、或NH3,合理即可)
CuSO4+2H2O+ SO2↑ 漂白 溶液由无色变成红色 SO2+2OH-=SO32-+H2O NO2(或Cl2、或O2、或NH3,合理即可)
【解析】
(1)装置A中铜与浓硫酸在加热的条件下反应生成硫酸铜、二氧化硫和水;
(2)SO2具有漂白性,可使品红溶液褪色,但不稳定;
(3)装置C中试管口的棉花团中浸有的NaOH溶液,可与二氧化硫反应生成亚硫酸钠和水;
(4)SO2与氯化钡不反应,若产生白色沉淀,可有2种途径,一使溶液显碱性,生成亚硫酸钡;二氧化SO2,生成硫酸钡。
(1)装置A中铜与浓硫酸在加热的条件下反应生成硫酸铜、二氧化硫和水,方程式为Cu+2H2SO4(浓)![]() CuSO4+2H2O+ SO2↑;
CuSO4+2H2O+ SO2↑;
(2)SO2具有漂白性,可使品红溶液褪色,但不稳定,在加热时还原,即溶液由无色变成红色;
(3)装置C中试管口的棉花团中浸有的NaOH溶液,可与二氧化硫反应生成亚硫酸钠和水,反应的离子方程式为SO2+2OH-=SO32-+H2O;
(4)SO2与氯化钡不反应,若产生白色沉淀,可有2种途径,一使溶液显碱性,生成亚硫酸钡;二氧化SO2,生成硫酸钡,则答案为NO2(或Cl2、或O2、或NH3,合理即可)。

 阅读快车系列答案
阅读快车系列答案【题目】(1)某溶液中含有SO42-、CO32-、Cl-,若只允许取一次该溶液而把三种离子分别检验出来,则应采取的措施是:
①先加入_____________检验_____________________;
②然后加入_________________,检验_____________;
③最后加入______________检验____________________________。
(2)阅读、分析下列两个材料:
材料一、(见图)
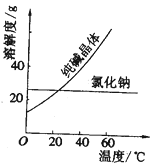
材料二、
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm3 | 溶解性 |
乙二醇( C2H6O2) | 11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
回答下列问题(填写序号):
A.蒸馏法 B.萃取法
C.“溶解、结晶、过滤”的方法 D.分液法
①纯碱从氯化钠和纯碱的混合物中分离出来,最好应用______。
②将乙二醇和丙三醇相互分离的最佳方法是__________。