题目内容
【题目】利用分类和氧化还原反应的知识能实现物质的转化。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:浓硫酸、I2、NaOH、NaCl、HCl
①HBr→Br2的化学方程式:___;
②V2O5(酸性氧化物)→VO![]() 的离子方程式:___。
的离子方程式:___。
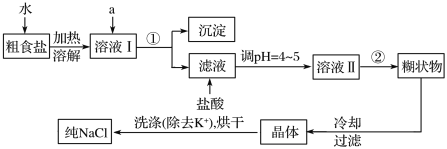
(2)利用含碘酸性废水(其中碘主要以IO![]() 形式存在)为原料生产CuI,其流程如图:
形式存在)为原料生产CuI,其流程如图:

①写出“反应Ⅰ”的离子方程式为___;
②写出“反应Ⅱ”的离子方程式:___。
【答案】2HBr+H2SO4(浓)=SO2↑+Br2+2H2O V2O5+6OH-=2VO![]() +3H2O IO
+3H2O IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+ 4I-+2Cu2+=2CuI↓+I2
+I-+6H+ 4I-+2Cu2+=2CuI↓+I2
【解析】
(1)①HBr→Br2过程中需要加入氧化剂反应把HBr氧化为Br2,据此分析;
②V2O5为酸性氧化物,在碱性溶液中反应生成相应的可溶性盐而电离出VO![]() ,据此分析;(2)含碘酸性废水中碘主要以IO
,据此分析;(2)含碘酸性废水中碘主要以IO![]() ,加入过量的SO2,会发生离子反应IO
,加入过量的SO2,会发生离子反应IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+;反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,过滤即可得到CuI 和含I2的滤液,据此分析。
+I-+6H+;反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,过滤即可得到CuI 和含I2的滤液,据此分析。
(1)①HBr→Br2过程中需要加入氧化剂浓硫酸反应把HBr氧化为Br2,其化学方程式为2HBr+H2SO4(浓)=SO2↑+Br2+2H2O,故答案为:2HBr+H2SO4(浓)=SO2↑+Br2+2H2O;
②V2O5为酸性氧化物,在碱性溶液中反应生成VO![]() ,其离子方程式为V2O5+6OH-=2VO
,其离子方程式为V2O5+6OH-=2VO![]() +3H2O,故答案为:V2O5+6OH-=2VO
+3H2O,故答案为:V2O5+6OH-=2VO![]() +3H2O;
+3H2O;
(2)含碘酸性废水中碘主要以IO![]() ,加入过量的SO2,会发生离子反应IO
,加入过量的SO2,会发生离子反应IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+,反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,故答案为:IO
+I-+6H+,反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,故答案为:IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+;4I-+2Cu2+=2CuI↓+I2。
+I-+6H+;4I-+2Cu2+=2CuI↓+I2。

 名校课堂系列答案
名校课堂系列答案