��Ŀ����
����Ŀ��ʳ�����ճ�����ı���Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϡ�
��1����ʳ���г���������K����Ca2����Mg2����![]() ���������ӣ�ʵ�����ᴿNaCl���������£�
���������ӣ�ʵ�����ᴿNaCl���������£�
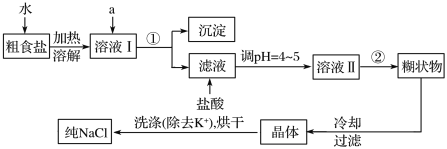
�ṩ���Լ�������Na2CO3��Һ������K2CO3��Һ��NaOH��Һ��BaCl2��Һ��Ba(NO3)2��Һ
��1�������γ�ȥ��Һ���е�Mg2����![]() ��Ca2����ѡ��a���������Լ������μ�˳������Ϊ_______��Һ��_________��Һ��_________��Һ��(�ѧʽ)��
��Ca2����ѡ��a���������Լ������μ�˳������Ϊ_______��Һ��_________��Һ��_________��Һ��(�ѧʽ)��
��2����������������õ��IJ����������˲��������ձ�������Ҫ__________________��
��3�������������__________________
��4��ʵ�����ォ�����Ƴɾ��εĹ����У����ܽ�IJ�����Ҫ�õ���������������Ϊ__________________
���𰸡�NaOH BaCl2 Na2CO3 ©�� ��ȥ�����NaOH��Na2CO3 ���衢�����ܽ�
��������
(1)Mg2+�ù�����NaOH��Һ��ȥ��![]() �ù�����BaCl2��Һ��ȥ��Ca2+�ù�����Na2CO3��ȥ���ʴ�Ϊ��NaOH��BaCl2��Na2CO3��
�ù�����BaCl2��Һ��ȥ��Ca2+�ù�����Na2CO3��ȥ���ʴ�Ϊ��NaOH��BaCl2��Na2CO3��
(2)������Ϊ���ˣ������������˲��������ձ�������Ҫ©�����ʴ�Ϊ��©����
(3)�ڳ�Mg2����![]() ��Ca2��ʱ�������˹�����NaOH��BaCl2��Na2CO3�����У�BaCl2���ɹ�����Na2CO3��ȥ�������NaOH��Na2CO3δ��ȥ����������Ϊ�˳�ȥ�����NaOH��Na2CO3���ʴ�Ϊ����ȥ�����NaOH��Na2CO3��
��Ca2��ʱ�������˹�����NaOH��BaCl2��Na2CO3�����У�BaCl2���ɹ�����Na2CO3��ȥ�������NaOH��Na2CO3δ��ȥ����������Ϊ�˳�ȥ�����NaOH��Na2CO3���ʴ�Ϊ����ȥ�����NaOH��Na2CO3��
(4)�ܽ��õ��������������ǽ��衢�����ܽ⣬�ʴ�Ϊ�����衢�����ܽ⡣

����Ŀ���¶�ΪTʱ����2.0L�����ܱ������г���1.0 mol PCl5����ӦPCl5(g)![]() PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ����
PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ����
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A����Ӧ��ǰ50 s��ƽ������Ϊv(PCl3)=0.0032mol��L��1��s��1
B�����������������䣬�����¶ȣ�ƽ��ʱc(PCl3)=0.11mol��L��1����Ӧ����H��0
C����ͬ�¶��£���ʼʱ�������г���1.0mol PCl5��0.20mol PCl3��0.20molCl2���ﵽƽ��ǰv(��)��v(��)
D����ͬ�¶��£���ʼʱ�������г���2.0mol PCl3��2.0molCl2���ﵽƽ��ʱ��PCl3��ת����С��80%