题目内容
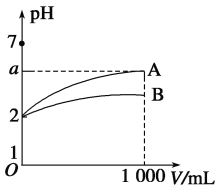
【题目】室温下,pH=2的A、B两种酸溶液各1 mL,分别加水稀释到1 000 mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法中正确的是
A. A、B两种酸溶液物质的量浓度一定相等
B. 稀释后A酸溶液的酸性比B酸溶液强
C. 若A、B都是弱酸,则6>a>2
D. 当a=5时,A是强酸,B是弱酸
【答案】D
【解析】
酸液稀释1000倍,强酸中不存在电离平衡,因此c(H+)变为原溶液的1/1000,即pH增大3个单位;而弱酸中存在电离平衡,稀释时电离平衡正向移动,导致c(H+)减小程度小于稀释的倍数,即pH的增大小于3个单位,据此解题。
A、室温下,pH=2的A、B两种酸溶液酸液稀释1000倍,A溶液pH变化较B大,说明两者酸性不同,即电离程度不同,若A、B两种酸pH=2,则浓度一定不相等,故A错误;
B、稀释后A酸的pH更大,说明c(H+)比B小,因此稀释后A酸溶液的酸性比B酸溶液弱,故B错误;
C、若A、B都是弱酸,弱酸中存在电离平衡,稀释时电离平衡正向移动,导致c(H+)减小程度小于稀释的倍数,所以pH的增大小于3个单位,即5>a>2,故C错误;
D、A、B两种酸分别稀释1000倍,强酸中不存在电离平衡,因此c(H+)变为原溶液的1/1000,即pH增大3个单位,若a=5,则A是强酸;而弱酸中存在电离平衡,稀释时电离平衡正向移动,导致c(H+)减小程度小于稀释的倍数,即pH的增大小于3个单位,从图中可知B稀释后pH小于a,所以B为弱酸,故D正确;
综上所述,本题应选D。

【题目】根据下列五种短周期元素的电离能数据(单位:kJ/mol),回答下面各题。
元素代号 | I1 | I2 | I3 | I4 | I5 |
Q | 800.6 | 2427.1 | 3659.7 | 25025.8 | 32826.7 |
R | 495.8 | 4562 | 6910.3 | 9543 | 13354 |
S | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
T | 1402.3 | 2856 | 4578.1 | 7475.0 | 9444.9 |
U | 2080.7 | 3952.3 | 6122 | 9371 | 12177 |
(1)在这五种元素中,最可能处于同一族的两种元素是_________(填元素符号),S元素最可能是_____区元素
(2)基态Q元素原子的价电子排布式是____________。Q和T同周期。化合物QT中T元素的化合价为_______;第一电离能介于Q、T之间的同周期元素有______种。
(3)化合物RT3中化学键类型为_______,RT3的阴离子的几何构型为________。
(4)下列元素中,化学性质和物理性质最像U元素的是_____________
A.硼 B.铍 C.锂 D.氦 E.碳
(5)R的某种氧化物X晶胞结构如图所示,晶胞参数a=0.566 nm,X的化学式为_____;列式并计算晶体X的密度(g·cm-3)_____。