题目内容
9.丁基羟基茴香醚(简称BHA )为食品抗氧剂,其结构简式如图1(1)BHA的分子式为C11H16O2,作抗氧剂的原因可能是含有酚羟基(填官能团名称).
(2)BHA可发生的反应为取代反应、氧化反应、加成反应 (填反应类型)
(3)A为BHA的同分异构体,存在图2转化,其中E用于液晶聚合物和塑料.
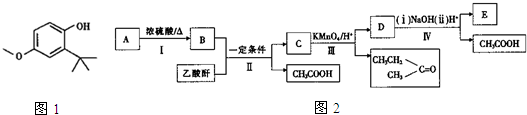
已知:I、A、B、C、D、E都是苯的对位二元取代物,A、B、E遇FeCl3溶液呈紫色
Ⅱ、
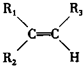 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$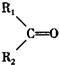 +R3COOH
+R3COOHⅢ、R-OH+
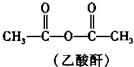 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +CH3COOH
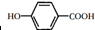
+CH3COOH①E的结构简式为
②写出符合以下条件的B的同分异构体的结构简式:
ⅰ)能发生银镜反应;
ii) 是苯的间位三元取代物,有两个相同的取代基,且含有三个甲基.
③反应II的化学方程式为
 ;反应II和IV的目的是保护B中的羟基,防止被酸性高锰酸钾氧化.
;反应II和IV的目的是保护B中的羟基,防止被酸性高锰酸钾氧化.
分析 (1)根据BHA的结构简式可知其分子式,BHA中含有酚羟基,易被氧化,可以作抗氧剂;
(2)BHA分子中含有酚羟基,具有酚的性质,具有苯环,可以发生加成反应;
(3)A为BHA的同分异构体,A、B、C、D、E都是苯的对位二元取代物,A、B、E遇FeCl3溶液呈紫色,均含有酚羟基,由反应Ⅱ及反应Ⅲ的产物可知B中侧链为-CH=C(CH3)CH2CH3,则B为 ,则C为
,则C为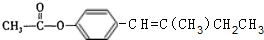 ,D为
,D为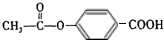 ,故E为
,故E为 ,据此解答.
,据此解答.
解答 解:(1)根据BHA的结构简式可知其分子式为C11H16O2,BHA中含有酚羟基,易被氧化,可以作抗氧剂,故答案为:C11H16O2;酚羟基;
(2)BHA分子中含有酚羟基,具有酚的性质,可以发生取代反应、氧化反应,具有苯环,可以发生加成反应,
故答案为:取代反应、氧化反应、加成反应;
(3)A为BHA的同分异构体,A、B、C、D、E都是苯的对位二元取代物,A、B、E遇FeCl3溶液呈紫色,均含有酚羟基,由反应Ⅱ及反应Ⅲ的产物可知B中侧链为-CH=C(CH3)CH2CH3,则B为 ,则C为
,则C为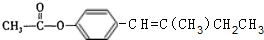 ,D为
,D为 ,故E为
,故E为 ,
,
①由上述分析可知,E的结构简式为 ,故答案为:
,故答案为: ;
;
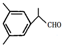
②符合以下条件的B( )的同分异构体:(i)能发生银镜反应,含有-CHO,(ii)是苯的间位三元取代物,有两个相同的取代基,且含有三个甲基,则三个取代基为-CH(CH3)CHO、2个-CH3,该同分异构体为
)的同分异构体:(i)能发生银镜反应,含有-CHO,(ii)是苯的间位三元取代物,有两个相同的取代基,且含有三个甲基,则三个取代基为-CH(CH3)CHO、2个-CH3,该同分异构体为 ,
,
故答案为: ;
;
③反应II的化学方程式为: ,反应Ⅲ中使用酸性高锰酸钾氧化碳碳双键,也可以氧化酚羟基,设计反应II和IV的目的是:保护B中的羟基,防止被酸性高锰酸钾氧化,
,反应Ⅲ中使用酸性高锰酸钾氧化碳碳双键,也可以氧化酚羟基,设计反应II和IV的目的是:保护B中的羟基,防止被酸性高锰酸钾氧化,
故答案为: ;保护B中的羟基,防止被酸性高锰酸钾氧化.
;保护B中的羟基,防止被酸性高锰酸钾氧化.
点评 本题考查有机物推断与合成、有机物结构与性质、同分异构体等,需要学生对给予的信息进行利用,能较好的考查学生自学能力与知识迁移运用能力,充分理解给予的信息是关键,对学生的推理能力有一定的要求,难度中等.

| A. | 同一主族元素,原子半径越大,其单质的熔点不一定越高 | |
| B. | 全部由非金属元素组成的化合物中一定只有共价键 | |
| C. | 在由锌片、铜片、稀硫酸组成的原电池中,电子由铜片经外电路流向锌片 | |
| D. | 氯化钠和氯化氢分别溶解在水中所克服的粒子间相互作用属于同种类型 |
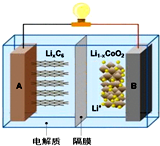 全电动汽车使用的是钴酸锂电池,其工作原理如图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2.则有关说法不正确的是( )
全电动汽车使用的是钴酸锂电池,其工作原理如图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2.则有关说法不正确的是( )| A. | 放电时电子从A极通过导线流向B极有关 | |
| B. | 放电时A是负极,电极反应式为:LixC6-xe-=C6+xLi+ | |
| C. | 充电时Li+从左边流向右边 | |
| D. | 充电时B作阳极,电极反应式为:LiCoO2-xe-=Li1-xCoO2+xLi+ |
| A. | NaHA溶液一定呈酸性 | B. | c(H+)•c(OH-)=1×10-14x | ||
| C. | c(Na+)=c(K+) | D. | c(Na+)+c(K+)=0.05 mol/L |
| A. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 | |
| C. | 铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| D. | HNO3→NO→NO2,以上各步变化均能通过一步实现 |
| A. | 稀硝酸、稀硫酸均能将木炭氧化成二氧化碳 | |
| B. | Na2O2与水反应,红热的Fe与水蒸气反应均能生成气体 | |
| C. | Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物 | |
| D. | NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
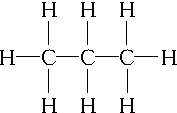 ,C3H6的同分异构体为CH2═CH-CH3、
,C3H6的同分异构体为CH2═CH-CH3、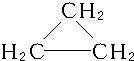 .
.