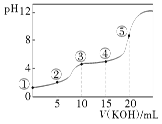题目内容
【题目】常温下,浓度均为![]() 、体积均为
、体积均为![]() 的NaX、NaY溶液分别加水稀释至体积为
的NaX、NaY溶液分别加水稀释至体积为![]() 与
与![]() 的变化关系如图所示。已知
的变化关系如图所示。已知![]() 。下列说法不正确的是( )
。下列说法不正确的是( )

A.水的电离程度a点大于b点
B.HX、HY都是弱酸,且![]()
C.![]() 时,NaX溶液所含离子总数大于NaY溶液
时,NaX溶液所含离子总数大于NaY溶液
D.分别向稀释前的两种溶液中加入盐酸至![]() ,
,![]()
【答案】D
【解析】
A.NaX、NaY溶液水解溶液呈碱性,促进了水的电离,溶液碱性越强,水的电离程度越大,根据![]() 可知,pOH越大溶液碱性越弱,根据图象可知,pOH:
可知,pOH越大溶液碱性越弱,根据图象可知,pOH:![]() ,则水的电离程度a点大于b点,故A正确;
,则水的电离程度a点大于b点,故A正确;
B.图象可知NaX、NaY溶液pOH大小![]() ,说明碱性
,说明碱性![]() ,当
,当![]() 时,NaY溶液pOH变化大,说明
时,NaY溶液pOH变化大,说明![]() 离子水解程度大,对应酸的酸性
离子水解程度大,对应酸的酸性![]() ,酸性越强电离平衡常数越大,则电离平衡常数:
,酸性越强电离平衡常数越大,则电离平衡常数:![]() ,故B正确;
,故B正确;
C.当![]() 时,NaY溶液的pOH较小,则说明
时,NaY溶液的pOH较小,则说明![]() 离子水解程度较大,NaX溶液中电荷守恒
离子水解程度较大,NaX溶液中电荷守恒![]() ,NaY溶液中电荷守恒
,NaY溶液中电荷守恒![]() ,两溶液中阳离子总浓度为
,两溶液中阳离子总浓度为![]() ;由于NaX溶液中
;由于NaX溶液中![]() 小于NaY溶液中
小于NaY溶液中![]() ,则
,则![]() :
:![]() ,两溶液中
,两溶液中![]() 相同,则NaX溶液中所含离子总数大于NaY溶液,故C正确;
相同,则NaX溶液中所含离子总数大于NaY溶液,故C正确;
D.向稀释前的两溶液中分别加盐酸至![]() 时,根据电荷守恒可知:
时,根据电荷守恒可知:![]() 、
、![]() ,盐溶液的pOH:
,盐溶液的pOH:![]() ,反应后溶液为中性时,NaY溶液消耗盐酸多,反应后溶液中
,反应后溶液为中性时,NaY溶液消耗盐酸多,反应后溶液中![]() :
:![]() ,则
,则![]() ,故D错误;
,故D错误;
答案选D。

练习册系列答案
 能力评价系列答案
能力评价系列答案
相关题目