题目内容
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知![]() ,下列有关叙述错误的是( )
,下列有关叙述错误的是( )
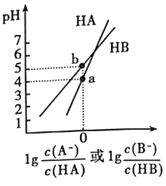
A.HA、HB两种酸中,HB的酸性弱于HA
B.b点时,![]()
C.同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,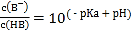
【答案】C
【解析】
A.当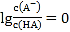 时,
时,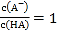 ,
, ,同理
,同理![]() ,相同温度下,酸的电离平衡常数越大,酸的酸性越强,因为
,相同温度下,酸的电离平衡常数越大,酸的酸性越强,因为![]() ,所以酸性
,所以酸性![]() ,故A正确;
,故A正确;
B.b点时,横坐标为0,则![]() ,溶液
,溶液![]() ,溶液呈酸性,则
,溶液呈酸性,则![]() ,溶液中存在电荷守恒,根据电荷守恒得
,溶液中存在电荷守恒,根据电荷守恒得![]() ,溶液中
,溶液中![]() 较小,所以存在
较小,所以存在![]() ,故B正确;
,故B正确;
C.根据A知,酸性![]() ,则水解程度
,则水解程度![]() ,所以相同浓度相同体积的NaA和NaB溶液中
,所以相同浓度相同体积的NaA和NaB溶液中![]() :
:![]() ,温度相同水的离子积常数相同,则这两种溶液中
,温度相同水的离子积常数相同,则这两种溶液中![]() :
:![]() ,溶液中分别存在电荷守恒
,溶液中分别存在电荷守恒![]() 、
、![]() ,根据物料守恒得两种溶液中
,根据物料守恒得两种溶液中![]() 相等,所以
相等,所以![]() :
:![]() ,根据电荷守恒知,阴离子浓度总数
,根据电荷守恒知,阴离子浓度总数![]() ,故C错误;
,故C错误;
D. ,则
,则 ,故D正确;
,故D正确;
答案选C。

【题目】温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)===PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A. 反应在前50 s的平均速率v(PCl3)=0.0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0
C. 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
【题目】【化学—选修3:物质结构与性质】第四周期过渡元素Mn、Fe、Ti、Ni可与C、H、O形成多种化合物。
(1)下列叙述正确的是 。(填字母)
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个![]() 键和1个大
键和1个大![]() 键,C6H6是非极性分子
键,C6H6是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
元 素 | Mn | Fe | |
电离能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
Mn原子价电子排布式为 ,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是 。
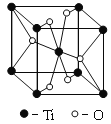
(3)根据元素原子的外围电子排布,可将元素周期表分区,其中Ti属于____________区。Ti的一种氧化物X,其晶胞结构如上图所示,则X的 化学式为 。
(4)某铁的化合物结构简式如右图所示
①组成上述化合物中各非金属元素电负性由大到小的顺序为
(用元素符号表示)
②在右图中用“→”标出亚铁离子的配位键。

(5)NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的配位数为 ,这几个O2-构成的空间构型为 。已知Ni2+与O2-的核间距为anm, NiO的摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则该晶体的密度为________ g/cm3。