题目内容
【题目】自来水生产的流程示意图见下:

(1)二氧化氯(ClO2)是一种高效、安全的水处理剂,比C12好。有如下两种制备C1O2方法:
方法一:2NaClO3+4HCl=2C1O2↑+Cl2↑+2NaCl+2H2O
方法二:2NaC lO3 +H2O2+H2SO4=2C lO2↑ +Na2SO4十O2↑+2H2O
用方法二制备的C1O2更适合用于饮用水消毒,其主要原因是__________。
C1O2和C12在消毒时自身均被还原为Cl-, C1O2的消毒能力是等质量Cl2的_________倍
(2)含有较多的钙、镁离子的水被称为硬水。暂时硬水最常见的软化方法是_________。
永久硬水一般可以使用离子交换树脂软化,先把水通过装有_________ (填“阴”或“阳”)离子交换树脂的交换柱,再通过另一种功能的离子交换树脂。使用后的阳离子交换树脂可以置于_________中再生。
(3)水处理中常见的混凝剂有硫酸铝、聚合氛化铝、硫酸亚铁、硫酸铁等。硫酸亚铁作为混凝剂在除去悬浮物质时,需要将水的pH调至9左右,原因是_________。
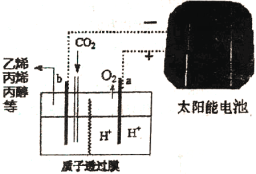
(4)电渗析法是一种利用离子交换膜进行海水淡化的方法.下图是电渗析法的示意图,淡水从_________(填“A”、“B”或,“C”)口流出,甲为_________离子交换膜。

【答案】(1)方法二制备的ClO2中不含Cl2;2.63;
(2)加热煮沸;阳;5%~8%的食盐水;
(3)Fe2+水解后的Fe(OH)2的溶解度大,混凝效果不好,需要在弱碱性下使用空气将Fe2+氧化为Fe3+,从而水解产生Fe(OH)3,起到较好的混凝效果;
(4)B;阴;
【解析】
试题分析:(1)因方法一制得的ClO2中含有Cl2,则用方法二制备的ClO2更适合用于饮用水的消毒,ClO2 的消毒效率(等质量时得到电子的多少)是Cl2 的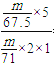 =2.63倍,故答案为:方法一制得的ClO2中含有Cl2;2.63;
=2.63倍,故答案为:方法一制得的ClO2中含有Cl2;2.63;
(2)加热煮沸是最常见的软化暂时硬水的方法,永久硬水一般可以使用离子交换树脂软化,先把水通过装有阳离子交换树脂的交换柱,再通过另一种功能的离子交换树脂。使用后的阳离子交换树脂可以置于5%~8%的食盐水中再生,故答案为:加热煮沸; 阳; 5%~8%的食盐水;
(3)Fe2+水解后的Fe(OH)2的溶解度大,混凝效果不好,需要在弱碱性下使用空气将Fe2+氧化为Fe3+,从而水解产生Fe(OH)3,起到较好的混凝效果,因此硫酸亚铁作为混凝剂在除去悬浮物质时,需要将水的pH调至9左右,故答案为:Fe2+水解后的Fe(OH)2的溶解度大,混凝效果不好,需要在弱碱性下使用空气将Fe2+氧化为Fe3+,从而水解产生Fe(OH)3,起到较好的混凝效果;
(4)两膜中间溶液中的氯离子向阳极移动,钠离子向阴极移动,所以B是淡水出口,因此甲为阴离子交换膜,故答案为:B;阴。