题目内容
2.S2Cl2是一种金黄色易挥发的液体,常用作橡胶硫化剂.某化学兴趣小组 拟设计实验制备少量的S2Cl2,査阅资料知S2Cl2在水中易发生歧化反应(一部分硫元素化 合价升高,另一部分化合价降低).加热条件下硫单质和干燥、纯净的Cl2反应即可生成S2Cl2,反应的化学方程式为:2S+Cl2$\frac{\underline{\;95~100℃\;}}{\;}$S2Cl2.反应涉及的几种物质的熔沸点如下:
| 物质 | S | S2Cl2 |
| 沸点/℃ | 445 | 138 |
| 熔点/℃ | 113 | -76 |
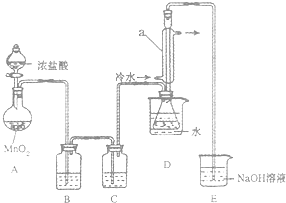 该小组设计的制备装置如图(夹持仪器已略去),回答下列问题:
该小组设计的制备装置如图(夹持仪器已略去),回答下列问题:(1)连接好实验装置后的第一步实验操作是检查装置的气密性.
(2)实验中需要加热的仪器是AD.(填写字母)
(3)装置B、C中的试剂分别是饱和食盐水、浓硫酸.
(4)装置D中仪器a的作用是冷凝回流、导气.
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏.
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气 体产生.用离子方程式表示产生该现象的原因ClO-+2H++Cl-=Cl2↑+H2O.
分析 制取原理是:先是二氧化锰和浓盐酸之间反应得到氯气,但是氯气中混有HCl和水,应该先用饱和食盐水除去HCl,再用浓硫酸干燥氯气,让氯气和硫在一定温度下发生反应:2S+Cl2$\frac{\underline{\;95~100℃\;}}{\;}$S2Cl2,为了控制反应的温度,采用热水浴加热的方法,根据S2Cl2的熔沸点数据,采用冷凝回流的办法将之收集即可试验中的氯气要进行尾气处理,可以用氢氧化钠来吸收,据此答题.
解答 解:制取原理是:先是二氧化锰和浓盐酸之间反应得到氯气,但是氯气中混有HCl和水,应该先用饱和食盐水除去HCl,再用浓硫酸干燥氯气,让氯气和硫在一定温度下发生反应:2S+Cl2$\frac{\underline{\;95~100℃\;}}{\;}$S2Cl2,为了控制反应的温度,采用热水浴加热的方法,根据S2Cl2的熔沸点数据,采用冷凝回流的办法将之收集即可试验中的氯气要进行尾气处理,可以用氢氧化钠来吸收,
(1)由于装置中有气体产生和反应,所以连接好实验装置后的第一步实验操作是检查装置的气密性,
故答案为:检查装置的气密性;
(2)浓盐酸与二氧化锰制氯气需要加热,氯气和二硫化碳反应应控制在95~100℃,要用水浴加热,所以实验中需要加热的仪器是AD,
故答案为:AD;
(3)根据上面的分析可知,装置B、C中的试剂分别是饱和食盐水、浓硫酸,
故答案为:饱和食盐水、浓硫酸;
(4)装置D中仪器a是冷凝管,其作用是冷凝回流、导气,
故答案为:冷凝回流、导气;
(5)反应结束后从锥形瓶内混合物主要为S2Cl2和S的混合物,根据题中信息可知,S2Cl2和S的沸点不同,所以从混合物中分离出产品的方法是蒸馏,
故答案为:蒸馏;
(6)若实验过程中缺少C装置,不经过干燥,氯气中有水,S2Cl2与水反应,有黄色单质硫沉淀生成,反应的化学方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑,
故答案为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑;
(7)E烧杯中吸收了氯气的氢氧化钠溶液中含有氯化钠、次氯酸钠,向其中加入浓盐酸,则在酸性环境下,氯离子和次氯酸根离子之间可以发生归中反应得到氯气,反应为:ClO-+2H++Cl-=Cl2↑+H2O,
故答案为:ClO-+2H++Cl-=Cl2↑+H2O.
点评 本题考查了氯气实验室制备方法,杂质气体除杂的装置选择和试剂选择,题干信息的应用分析,电子式书写,化学方程式书写方法,混合物分离的方法判断,题目难度中等.

| A. | 1.0 L mol/L NaCl溶液中含有Cl-约为6.02×10-23 | |
| B. | 配制一定物质的量浓度的溶液,用浓硫酸配制稀硫酸与用NaOH固体配制NaOH溶液使用的仪器是不同的 | |
| C. | 把1L 2mol/L的盐酸稀释为1mol/L的盐酸需要加入1L的蒸馏水 | |
| D. | 25℃可以配制1.0mol/L的Ba(OH)2溶液[Ba(OH)2•8H2O在293K和303K时的溶解度分别为3.9g和5.6g] |
| A. | 该温度下KOH的溶解度为$\frac{2a}{1-2a%}$g | |
| B. | 原溶液的质量为3mg | |
| C. | 可以求算原溶液的物质的量浓度 | |
| D. | 保持温度不变,向原溶液中加入2a g KOH可达饱和 |
| A. | 2.4g金属镁全部变成镁离子时失去的电子数为0.1NA | |
| B. | 1.0 mol任何单质气体的分子数均为NA,原子数均为2NA | |
| C. | 17gNH3所含的电子数目为NA | |
| D. | 16g 02和03混合气体中.含有原子数为NA |
(1)碱性:Sr(OH)2< Ba(OH)2(填“>”或“<”);锶的化学性质与钙和钡类似,用原子结构的观点解释其原因是同一主族元素,原子最外层电子数相同.
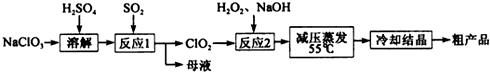
(2)碳酸锶是最重要的锶化合物.用含SrSO4和少量BaSO4、BaCO3、FeO、Fe2O3、Al2O3、SiO2的天青石制备SrCO3,工艺流程如下(部分操作和条件略):
Ⅰ.将天青石矿粉和Na2CO3溶液充分混合,过滤;
Ⅱ.将滤渣溶于盐酸,过滤;
Ⅲ.向Ⅱ所得滤液中加入浓硫酸,过滤;
Ⅳ.向Ⅲ所得滤液中先加入次氯酸,充分反应后再用氨水调pH约为7,过滤;
Ⅴ.向Ⅳ所得滤液中加入稍过量NH4HCO3,充分反应后,过滤,将沉淀洗净,烘干,得到SrCO3.
已知:ⅰ.相同温度时的溶解度:BaSO4<SrCO3<SrSO4<CaSO4
ⅱ.生成氢氧化物沉淀的pH
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀pH | 1.9 | 7.0 | 3.4 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 |
②Ⅱ中,能与盐酸反应溶解的物质有SrCO3、BaCO3、FeO、Fe2O3、Al2O3.
③Ⅳ的目的是将Fe2+氧化为Fe3+,使Fe3+和Al3+沉淀完全.
④下列关于该工艺流程的说法正确的是ac.
a.该工艺产生的废液含较多的NH4+、Na+、Cl-、SO42-
b.Ⅴ中反应时,升高温度一定可以提高SrCO3的生成速率
c.Ⅴ中反应时,加入溶液一定可以提高NH4HCO3的利用率.