题目内容
19.某温度下,将溶质质量分数为a%的KOH溶液蒸发掉mg水后恢复至原温度,恰好得到质量分数为2a%的KOH饱和溶液V mL,则下列说法中正确的是( )| A. | 该温度下KOH的溶解度为$\frac{2a}{1-2a%}$g | |
| B. | 原溶液的质量为3mg | |
| C. | 可以求算原溶液的物质的量浓度 | |
| D. | 保持温度不变,向原溶液中加入2a g KOH可达饱和 |
分析 A.饱和溶液的质量分数=$\frac{溶解度}{100+溶解度}$;
B.根据KOH的质量不变计算原KOH溶液的质量;
C.由V=$\frac{m}{ρ}$,c=$\frac{n}{V}$可以计算溶液物质的量浓度,但原溶液的密度不知,不能计算原溶液体积;
D.计算mg水可以溶解KOH的质量,据此判断.
解答 解:A.设该温度下KOH的溶解度为s g,则饱和溶液的质量分数=$\frac{s}{100+s}$×100%=2a%,解得s=$\frac{2a}{1-2a%}$,故A正确;
B.将溶质质量分数为a%的KOH溶液蒸发掉mg水后恢复至原温度,恰好得到质量分数为2a%的KOH饱和溶液,蒸发过程中只减少溶剂水,设原溶液的质量为xg,由溶质的质量守恒得:x×a%=(x-m)×2a%,解得x=2m,即原溶液的质量为2mg,故B错误;
C.由V=$\frac{m}{ρ}$,c=$\frac{n}{V}$可以计算溶液物质的量浓度,但原溶液的密度不知,不能计算原溶液体积,故物质的量浓度无法计算,故C错误;
D.溶解度为$\frac{200a}{100-2a}$g,则mg水可以溶解KOH的质量为$\frac{2a}{1-2a%}$g×$\frac{mg}{100g}$=$\frac{2ma}{100-2a}$g,该值不一定为2a g,故D错误,
故选:A.
点评 本题考查了溶液中溶质的质量分数、物质的量浓度的有关计算,难度不大,侧重于考查了学生的计算能力和对公式的应用能力,注意对溶解度的理解.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
10.实验室需要8.6%的氯化钠溶液100g,某同学用托盘天平称量氯化钠(不到1g的用游码),他把砝码放在左盘,氯化钠放在右盘,当天平平衡时,所称取的氯化钠的实际质量应是( )
| A. | 9.2g | B. | 8.6g | C. | 8g | D. | 7.4g |
14.下列叙述中,正确的是( )
| A. | 标准状况下,22.4L水所含的原子数目为3NA | |
| B. | 一定条件下,等物质的量甲烷和一氧化碳所含的分子数可能不相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 标准状况下,17g氨气的体积约为22.4L |
4.在Na2SO4和K2SO3混合溶液中,当c(Na+)=0.2mol•L-1,c(SO42-)=x mol•L-1,c(K+)=y mol•L-1时,x与y的关系是( )
| A. | x=y+0.2 | B. | x=$\frac{y}{2}$ | C. | x=0.1+$\frac{y}{2}$ | D. | x=y |
2.S2Cl2是一种金黄色易挥发的液体,常用作橡胶硫化剂.某化学兴趣小组 拟设计实验制备少量的S2Cl2,査阅资料知S2Cl2在水中易发生歧化反应(一部分硫元素化 合价升高,另一部分化合价降低).加热条件下硫单质和干燥、纯净的Cl2反应即可生成S2Cl2,反应的化学方程式为:2S+Cl2$\frac{\underline{\;95~100℃\;}}{\;}$S2Cl2.
反应涉及的几种物质的熔沸点如下:
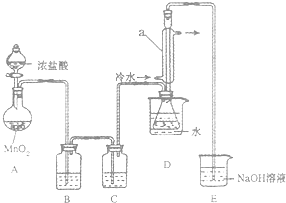 该小组设计的制备装置如图(夹持仪器已略去),回答下列问题:
该小组设计的制备装置如图(夹持仪器已略去),回答下列问题:
(1)连接好实验装置后的第一步实验操作是检查装置的气密性.
(2)实验中需要加热的仪器是AD.(填写字母)
(3)装置B、C中的试剂分别是饱和食盐水、浓硫酸.
(4)装置D中仪器a的作用是冷凝回流、导气.
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏.
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气 体产生.用离子方程式表示产生该现象的原因ClO-+2H++Cl-=Cl2↑+H2O.
反应涉及的几种物质的熔沸点如下:
| 物质 | S | S2Cl2 |
| 沸点/℃ | 445 | 138 |
| 熔点/℃ | 113 | -76 |
 该小组设计的制备装置如图(夹持仪器已略去),回答下列问题:
该小组设计的制备装置如图(夹持仪器已略去),回答下列问题:(1)连接好实验装置后的第一步实验操作是检查装置的气密性.
(2)实验中需要加热的仪器是AD.(填写字母)
(3)装置B、C中的试剂分别是饱和食盐水、浓硫酸.
(4)装置D中仪器a的作用是冷凝回流、导气.
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏.
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气 体产生.用离子方程式表示产生该现象的原因ClO-+2H++Cl-=Cl2↑+H2O.
20.常温下,下列各组微粒在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1 Fe(NO3)3溶液中:Mg2+、H+、SO42-、Cl- | |
| B. | 0.1 mol•L-1 KClO溶液中:Na+、H+、Cl-、NO3- | |
| C. | 0.1 mol•L-1氨水中:Ba2+、Ag+、NH4+、NO3- | |
| D. | c(OH-)=10-13 mol•L-1的溶液中:MnO4-、Na+、Br-、CH3CHO |