题目内容
17.原子序数依次增大的四种元素a、b、c、d,它们的最外层电子数分别为1、6、7、1,现有下列结构信息,a失去1个电子后,成为裸露的质子,b和c的次外层有8个电子,c-和d+的电子层结构相同.回答下列问题:(1)a、b、c、d依次为(填元素符号)aH bScCldK
(2)b、c元素的非金属性由强到弱的次序为Cl>S (填元素符号)
(3)c、d形成化合物的种类A(请选择)A离子化合物;B共价化合物,请写出该化合物的电子式
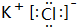
(4)b元素所形成的一种氧化物A既有氧化性又有还原性,A物质是(写化学式)SO2.在一个2L的密闭容器中,放入2mol A 气体与O2发生化学反应,5min后,测得气体A还剩余0.5mol,则该反应中,用气体A表示的化学反应速率是0.15mol/(L•min).
分析 原子序数依次增大的四种元素a、b、c、d,它们的最外层电子数分别为1、6、7、1,a失去1个电子后,成为裸露的质子,则a为H元素;b和c的次外层有8个电子,原子只能有3个电子层,则b为S元素,c为Cl,c-和d+的电子层结构相同,则d为K元素,据此解答.
解答 解:原子序数依次增大的四种元素a、b、c、d,它们的最外层电子数分别为1、6、7、1,a失去1个电子后,成为裸露的质子,则a为H元素;b和c的次外层有8个电子,原子只能有3个电子层,则b为S元素,c为Cl,c-和d+的电子层结构相同,则d为K元素.
(1)由上述分析可知,a为H、b为S、c为Cl、d为K,故答案为:H;S;Cl;K;
(2)同周期自左而右元素非金属性增强,故非金属性Cl>S,故答案为:Cl>S;
(3)c、d形成化合物为KCl,属于离子化合物,其电子式为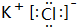 ,故答案为:A;
,故答案为:A;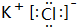 ;
;
(4)b元素(硫元素)所形成的一种氧化物A既有氧化性又有还原性,A物质是SO2,在一个2L的密闭容器中,放入2molSO2 气体与O2发生化学反应,5min后,测得气体SO2还剩余0.5mol,则该反应中,用气体SO2表示的化学反应速率是 $\frac{\frac{2mol-0.5mol}{2L}}{5min}$=0.15mol/(L•min),
故答案为:SO2;0.15mol/(L•min).
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对基础知识的理解掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.在浓硫酸催化并加热的条件下,CH3COOH与CH3CH218OH发生酯化反应时,分子中含有18O的生成物是( )
| A. | 水 | B. | 乙酸乙酯 | C. | 硫酸 | D. | 氧气 |
2.下列说法中,正确的是( )
| A. | 常温下,某NaHSO3溶液的pH<7,则该溶液中c(SO32-)<c(H2SO3) | |
| B. | 25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,所消耗溶液体积为:V(醋酸溶液)>V(NaOH溶液) | |
| C. | 将l mL pH=2的醋酸溶液加水稀释到10 mL,pH变为3 | |
| D. | 常温下,将Na2CO3溶液加水稀释,$\frac{{c({HC{O_3}^-})•c({O{H^-}})}}{{c({CO_3^{2-}})}}$的值增大 |
6.下列各组物质中,具有相同酸根的一组是( )
| A. | K2SO4、Na2SO3 | B. | K2MnO4、NaMnO4 | C. | CaCl2、NaCl | D. | NaCl、KClO3 |
7.下列各组物质的标准燃烧热相等的是( )
| A. | 碳和一氧化碳 | B. | 1mol碳和2mol碳 | ||
| C. | 1mol乙炔和2mol碳 | D. | 淀粉和纤维素 |

 .
.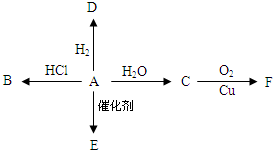 如图所示,已知有机物A的产量可以衡量一个国家的石油化工发展水平,A可以发生如图一系列的反应,按要求回答下列问题
如图所示,已知有机物A的产量可以衡量一个国家的石油化工发展水平,A可以发生如图一系列的反应,按要求回答下列问题