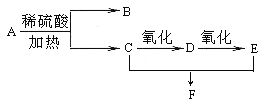
题目内容
【题目】碳酸二甲酯(简称DMC)是一种绿色化学品,可取代光气等有毒物质作为羰基化或甲基化试剂,如:
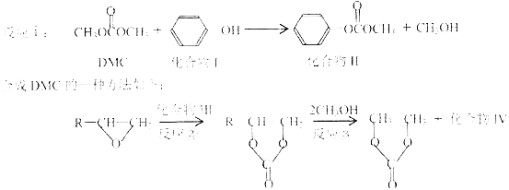
(1)化合物II核磁共振氢谱有 组峰;1mol该物质最多可以跟 mol氢气发生加成反应。
(2)反应①中副产物甲醇发生催化氧化反应的方程式为 。
(3)反应②原子利用率100%,则化合物Ⅲ的名称是 。化合物Ⅳ的结构简式是 ,反应③的反应类型是 。
(4)化合物V是化合物Ⅱ的一种同分异构体,其苯环上的一氯代物有两种,且能发生水解反应和银镜反应,则化合物V的结构简式为(写其中一种) 。
(5)一定条件下,![]() 与DMC 以物质的量之比为1∶1发生类似反应①的反应,请写出该反应的化学方程式 。
与DMC 以物质的量之比为1∶1发生类似反应①的反应,请写出该反应的化学方程式 。
【答案】
(1)4;3(2)![]()
(3)二氧化碳;![]() ;取代反应
;取代反应
(4)![]() 或
或![]() 或
或![]()
(5)![]()
【解析】
试题分析:(1)根据化合物Ⅱ的结构简式可知,化合物II核磁共振氢谱有4组峰;该物质中有一个苯环,所以1mol该物质可以跟3 mol氢气发生加成反应,故答案为:4;3;
(2)甲醇发生催化氧化后生成甲醛,所以反应①中副产物甲醇发生催化氧化反应的方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)反应②原子利用率100%,则根据元素守恒可写出Ⅲ的名称为二氧化碳,反应③是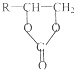 与甲醇发生取代反应,据此可写出Ⅳ的结构简式为
与甲醇发生取代反应,据此可写出Ⅳ的结构简式为![]() ,故答案为二氧化碳:
,故答案为二氧化碳:![]() ;取代反应;
;取代反应;
(4)化合物V是化合物Ⅱ的一种同分异构体,其苯环上的一氯代物有两种,且能发生水解反应和银镜反应,说明有酚羟基和酯基,据此写出结构简式为![]() 或
或![]() 或
或![]() ,故答案为:
,故答案为:![]() 或
或![]() 或
或![]() ;
;
(5)反应①为碳酸二甲酯中的甲基被取代,![]() 与DMC可以形成肽键,反应的化学方程式为
与DMC可以形成肽键,反应的化学方程式为![]() ,故答案为:
,故答案为:![]() 。
。

练习册系列答案
相关题目