题目内容
【题目】化合物A的分子式为C3H6O2,它有如下图所示转化关系,已知D、E、F在加热条件下都能与碱性新制Cu(OH)2悬浊液生成砖红色沉淀:
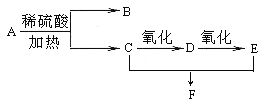
试回答下列问题:
(1)A的名称为 ,B所含官能团的名称为 ;
(2)写出A 生成B、C的化学反应方程式: ,
(3)写出C催化氧化为D的化学反应方程式: ;
(4)写出C和E生成F的化学反应方程式: ,反应类型是 。
【答案】
(1)乙酸甲酯,羧基;
(2)CH3COOCH3+H2O![]() CH3COOH+CH3OH;
CH3COOH+CH3OH;
(3)2CH3OH+O2![]() 2HCHO+2H2O;
2HCHO+2H2O;
(4)HCOOH+CH3OH![]() HCOOCH3+H2O;酯化反应或取代反应。
HCOOCH3+H2O;酯化反应或取代反应。
【解析】
试题分析:有机物C能连续被氧化,且C和E能发生反应生成F,则C为醇、D为醛、E为羧酸、F为酯,D、E、F都能发生银镜反应说明这三种物质中都含有醛基,则D的结构简式为HCHO、E的结构简式为HCOOH、F的结构简式为HCOOCH3、C的结构简式为CH3OH,A的分子式为C3H6O2,A发生水解反应生成B和C,C是甲醇,则B是乙酸,其结构简式为CH3COOH,A是乙酸甲酯,其结构简式为CH3COOCH3。
(1)通过以上分析知,A是乙酸甲酯,B是CH3COOH,B所含官能团的名称为羧基,故答案为:乙酸甲酯;羧基;
(2)A发生水解反应生成B和C,分液的化学反应方程式为CH3COOCH3+H2O![]() CH3COOH+CH3OH,故答案为:CH3COOCH3+H2O
CH3COOH+CH3OH,故答案为:CH3COOCH3+H2O![]() CH3COOH+CH3OH;
CH3COOH+CH3OH;
(3)C为CH3OH,C催化氧化为D的化学反应方程式为2CH3OH+O2![]() 2HCHO+2H2O,故答案为:2CH3OH+O2
2HCHO+2H2O,故答案为:2CH3OH+O2![]() 2HCHO+2H2O;
2HCHO+2H2O;
(4)在浓硫酸作催化剂、加热条件下,甲酸和甲醇发生酯化反应生成甲酸甲酯,反应方程式为:HCOOH+CH3OH![]() HCOOCH3+H2O,故答案为:HCOOH+CH3OH
HCOOCH3+H2O,故答案为:HCOOH+CH3OH![]() HCOOCH3+H2O;酯化反应。
HCOOCH3+H2O;酯化反应。

 备战中考寒假系列答案
备战中考寒假系列答案